题目内容
2.下列图象不能正确反映其对应关系的是( )| A. |  氯酸钾和二氧化锰混合加热制取氧气 | |
| B. | .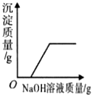 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 | |
| C. | .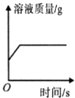 某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体. | |
| D. | .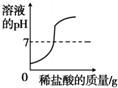 在氢氧化钠溶液中滴加稀盐酸 |
分析 A、根据二氧化锰是氯酸钾分解反应的催化剂进行分析解答;
B、根据氢氧化钠与硫酸优先反应解答;
C、根据饱和溶液的转化解答;
D、根据氢氧化钠和盐酸的反应解答.
解答 解:A、氯酸钾和二氧化锰混合加热制取氧气中二氧化锰是催化剂,质量不变,正确;
B、向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液,氢氧化钠与硫酸先反应,故沉淀过一段时间再出现,正确;
C、某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体,形成饱和溶液后质量不再改变,正确;
D、在氢氧化钠溶液中滴加稀盐酸,pH由大于7到小于7,错误;
故选D.
点评 本题考查的是常见的化学反应与图象的关系,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
4.兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(1)氢氧化钠固体要密封保存,原因有:
①氢氧化钠固体易潮解;②氢氧化钠与空气中二氧化碳反应变质.
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:
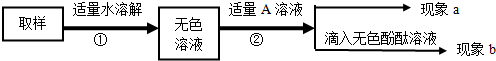
对无色溶液进行以下实验:
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:第一步氢氧化钙溶液与碳酸钠溶液反应生成氢氧化钠,干扰第二步氢氧化钠的检验.
④反思:把第一步中的氢氧化钙溶液换成氯化钙溶液,可达到实验目的.
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质.
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
(1)氢氧化钠固体要密封保存,原因有:
①氢氧化钠固体易潮解;②氢氧化钠与空气中二氧化碳反应变质.
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:

对无色溶液进行以下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡. | 现象a:白色沉淀 | 化学方程式: ①Na2CO3+Ca(OH)2=2NaOH+CaCO3↓,有碳酸钠并全部除尽. |
| 第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡. | 现象b: ②液体变红 | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
④反思:把第一步中的氢氧化钙溶液换成氯化钙溶液,可达到实验目的.
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质.
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
| 实验操作 | 实验现象 | 实验结论 |
5.NaCl和KNO3的溶解度如下,请回答下列问题.
(1)60℃时,KNO3的溶解度是110g;
(2)20℃时,将50g NaCl固体加入盛有100g水的烧杯中,充分溶解形成溶液的溶质质量分数是26.5%;
(3)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法是冷却热饱和溶液;
(4)将60℃等质量的KNO3的饱和溶液和NaCl的饱和溶液降温到20℃,分别得到溶液甲和乙.对所得溶液的叙述正确的是A,C(填序号).
A.都是饱和溶液 B.溶剂质量:甲>乙 C.溶液质量:甲<乙.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解 度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)20℃时,将50g NaCl固体加入盛有100g水的烧杯中,充分溶解形成溶液的溶质质量分数是26.5%;
(3)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法是冷却热饱和溶液;
(4)将60℃等质量的KNO3的饱和溶液和NaCl的饱和溶液降温到20℃,分别得到溶液甲和乙.对所得溶液的叙述正确的是A,C(填序号).
A.都是饱和溶液 B.溶剂质量:甲>乙 C.溶液质量:甲<乙.
7.下列图象能正确反映对应实验操作中量的关系是( )
| A. |  一定量稀硫酸加水稀释 | |
| B. |  一定量氯化铜和盐酸的混合溶液中逐渐加入稀硫酸 | |
| C. |  等质量的镁粉和铁粉中分别缓慢加入稀硫酸 | |
| D. |  等质量的高锰酸钾和氯酸钾加热制氧气 |
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,请回答下列问题:
”表示氧原子,请回答下列问题:
 根据图所示的装置,回答下列问题.
根据图所示的装置,回答下列问题.
 如图是某食盐说明书,KIO3中碘元素的化合价为+5,微量元素碘缺乏和过量都会引起甲状腺肿大,每袋食盐中含碘的质量为10mg.
如图是某食盐说明书,KIO3中碘元素的化合价为+5,微量元素碘缺乏和过量都会引起甲状腺肿大,每袋食盐中含碘的质量为10mg. 梅花5角硬币自1992年投放市场参与流通,至今已20多年.梅花5角硬币材料为黄铜,金黄色,圆形,边缘有间断丝齿.正面图案以梅花为主,图案右上方印有“5角”及其汉语拼音字样,背面图案以中华人民共和国国徽为主景,国徽上方印有汉语拼音国名,国徽下方印有国名和铸造年号.外缘内有圆点组成之圆圈,使币面显得更美观.请回答下列问题.
梅花5角硬币自1992年投放市场参与流通,至今已20多年.梅花5角硬币材料为黄铜,金黄色,圆形,边缘有间断丝齿.正面图案以梅花为主,图案右上方印有“5角”及其汉语拼音字样,背面图案以中华人民共和国国徽为主景,国徽上方印有汉语拼音国名,国徽下方印有国名和铸造年号.外缘内有圆点组成之圆圈,使币面显得更美观.请回答下列问题.