题目内容
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
解:设:略
(1)样品中氧化铁的质量是20g — 4 g == 16 g ……………………………… 1分
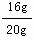
样品中,氧化铁的质量分数为 ×100% == 80%…………………… 1分
(2)Fe2 O3 + 6HCl===2 FeCl3 + 3H2O ……………………………………… 1分
160 325
16g X
 160 325
160 325
16g X
X == 32.5g …………………………………………………… 1分
所得溶液的质量为:184 g + 20 g — 4 g == 200 g …………………………… 1分
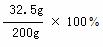 |
所得溶液中溶质的质量分数为 ==16.25% …………………………1分
答:略。
(单位和百分号都不在扣分范围内)

下列除去杂质的方法中,正确的是
| 选项 | 括号内为杂质 | 方 法 |
| A | CO2(HCl气体) | 通过足量的NaOH溶液 |
| B | KCl (KClO3) | 加入少量MnO2加热 |
| C | NaCl(Na2CO3) | 加入足量的盐酸后蒸干 |
| D | Fe(Cu) | 加入足量的稀H2SO4后过滤 |
下列有关溶液的说法中正确的是( )
|
| A | 常温下将100mL饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液 |
|
| B | 从浓度为25%的H2SO4溶液中取出10mL,则取出的10mL H2SO4溶液浓度仍为25% |
|
| C | 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克 |
|
| D | 将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的浓度为5% |
某同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究,请你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙;、
 猜想二:可能是CaCl2和Ca(OH)2;
猜想二:可能是CaCl2和Ca(OH)2;
猜想三: _________ .
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入 _________ 溶液至过量 | _________ | 猜想三正确 |
【方案评价】该同学与同学们通过讨论认为:
(1)方案一能证明猜想二正确,但不能证明猜想一正确.
(2)方案二可行.但该同学在记录时未记录完整,请你帮他将方案二补充完整.
【方案反思】方案一不能证明猜想一正确的理由是 _________ .
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是 _________ .
【结论】在分析化学反应后所得物质成分时,除考虑生成物外还需考虑 _________ .
 液与下列各物质恰好完全反应后,溶液仍显红色的是
液与下列各物质恰好完全反应后,溶液仍显红色的是 右图是某原子结构示意图,回答下列问题
右图是某原子结构示意图,回答下列问题