题目内容
2.过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解放出氧气,实验时,可以通过调节分液漏斗活塞控制液体的滴加速度,所用装置如图所示: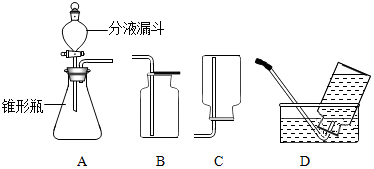
甲、乙两位同学要选用上述装置用过氧化氢溶液和二氧化锰制取氧气,试回答下列问题:
(1)分液漏斗中应加入的物质是过氧化氢溶液,锥形瓶中应放入的物质是二氧化锰,在该反应中起催化作用.
(2)甲、乙两位同学在制取气体时,都选用A装置作为气体发生装置,但其收集装置不相同,通过对比知道,甲收集的氧气纯度比乙高.则甲选D装置收集,乙选择B装置收集.
(3)甲同学选择该装置收集氧气的依据是氧气不易溶于水,他是如何知道已集满了一瓶氧气的集气瓶口有气泡冒出.
(4)乙同学选用收集装置的依据是氧气密度比空气大,证明氧气已集满的方法是把带火星的木条放在集气瓶口,木条复燃,证明集满.
(5)甲同学在实验开始时,观察到锥形瓶内有大量气泡产生,可收集装置中没有收集到氧气,其原因是装置气密性不好.
(6)欲证明二氧化锰在化学反应后化学性质没有发生变化,可采用的方法是反应后,产物沉淀过滤出来,烘干,称重,证明重量不变,再加入新的过氧化氢溶液,依然有氧气放出,依然能够起催化作用,再次将沉淀过滤出来,烘干,称重,证明重量依然不变.
(7)装置A中反应很剧烈,据此,甲、乙两位同学应采用的安全方法是①.
①控制液体流速 ②用体积小的锥形瓶 ③加热反应物.
分析 (1)根据分液漏斗可以用来添加液体,锥形瓶中直接加入固体,二氧化锰是过氧化氢分解的催化剂进行分析;
(2)(3)(4)根据排水法收集的氧气纯净,向上排空气法收集的氧气干燥,氧气密度比空气大,不易溶于水,氧气有助燃性进行分析;
(5)根据制取装置的气密性不好会造成装置漏气,收集不到气体进行分析;
(6)根据催化剂的定义:在化学反应中可以改变物质的反应速率,而本身的质量和化学性质都没有变化的物质叫催化剂进行分析;
(7)根据反应物接触越充分、浓度越大、温度越高,反应速率越快进行分析.
解答 解:(1)过氧化氢溶液是液体,二氧化锰是固体,分液漏斗可加入液体,所以分液漏斗中放入的是过氧化氢溶液,锥形瓶中放入的是二氧化锰,二氧化锰是过氧化氢分解的催化剂,在该反应中起催化作用;
(2)氧气不易溶于水且密度比空气大,所以可用排水法或向上排空气法收集,利用排水法收集的气体比排空气法收集的气体纯净,甲收集的氧气比乙纯说明甲用的是排水法,乙用的是向上排空气法收集;
(3)甲同学选择D装置收集氧气的依据是氧气不易溶于水,当集气瓶口有大气泡逸出时说明集气瓶已满;
(4)乙同学选用B收集装置的依据是氧气的密度比空气大,证明氧气已集满的方法是把带火星的木条放在集气瓶口,木条复燃,证明集满;
(5)有大量气泡生成,说明有氧气产生,可收集装置中没有收集到氧气,之所以没有收集到氧气,说明生成的氧气从其他地方跑掉了,装置漏气;
(6)反应后,产物沉淀过滤出来,烘干,称重,证明重量不变,再加入新的过氧化氢溶液,依然有氧气放出,依然能够起催化作用,再次将沉淀过滤出来,烘干,称重,证明重量依然不变;
(7)如要减慢装置A中的反应速率,应该减慢液体的滴加速率,减少反应物的量,而加热反应物能够加快反应速率,用体积较小的锥形瓶更容易发生安全事故,故选:①.
故答案为:(1)过氧化氢,二氧化锰,催化;
(2)D,B;
(3)氧气不易溶于水,集气瓶口有气泡冒出;
(4)氧气的密度比空气大,把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了;
(5)装置气密性不好;
(6)反应后,产物沉淀过滤出来,烘干,称重,证明重量不变,再加入新的过氧化氢溶液,依然有氧气放出,依然能够起催化作用,再次将沉淀过滤出来,烘干,称重,证明重量依然不变;
(7)①.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | Zn | B. | Cu | C. | Al | D. | Cu和Al |
| A | 食品保鲜的方法与原理 | B | 灭火实例与原理 |
| 放入固态二氧化碳-冷藏保鲜 放入生石灰-吸收水和氧气 充入氮气-防止氧化变质 | 用水浇灭火焰-降低着火点 用嘴吹灭蜡烛-隔绝空气 关闭燃气阀门-隔离可燃物 | ||
| C | 日常物质的区别 | D | 化学中常见的“三” |
| 硬水和软水-观察颜色 羊毛和涤纶-燃烧闻气味 纯铜片和黄铜片-互相刻划 | 三大化石燃料-煤、石油、沼气 三大合成材料-合金、塑料、合成纤维 三种构成物质的粒子-分子、原子、电子 |
| A. | A | B. | B | C. | C | D. | D |

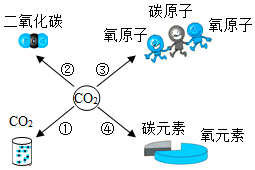 模型可以反映客观现象,简单明了地表示事物.如图是二氧化碳的化学式“CO2”所表达信息的模型.请选择两个编号并写出它所表达的信息:
模型可以反映客观现象,简单明了地表示事物.如图是二氧化碳的化学式“CO2”所表达信息的模型.请选择两个编号并写出它所表达的信息: