题目内容
6.实验室废液是造成水资源污染的原因之一.课外小组的同学在探究金属的性质后对含有CuSO4、FeSO4、ZnSO4和H2SO4的废液进行处理,其简单流程如下: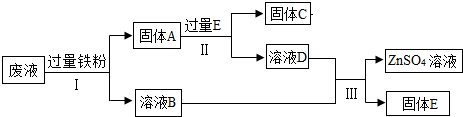
回答下列问题:
(1)步骤I中观察到的现象是有气泡产生,溶液由蓝色变为浅绿色.
(2)步骤Ⅱ中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(3)步骤Ⅲ应进行的操作是加入适量的锌粉、过滤.
分析 (1)根据铁与稀硫酸、硫酸铜的反应分析反应的现象;
(2)根据铁与硫酸的反应写出反应的化学方程式;
(3)根据要得到硫酸锌应将过量的硫酸和硫酸亚铁除去分析应加入的药品和操作.
解答 解:由题意可知,向含有CuSO4、FeSO4、ZnSO4和H2SO4的废液中加入过量的铁粉,铁与硫酸、硫酸铜发生了反应,过滤得到的固体A中含有铁和铜,溶液B中含有硫酸亚铁和硫酸锌;为了将固体A中的铁除去,应加入过量的稀硫酸,过滤得到了溶液D中含有硫酸亚铁、硫酸和硫酸锌溶液,为了将硫酸亚铁和硫酸除去,应加适量的锌粉再过滤就得到了硫酸锌和铁.
(1)由上述分析可知,步骤I中铁与硫酸、硫酸铜发生了反应,观察到的现象是:有气泡产生,溶液由蓝色变为浅绿色.
(2)由上述分析可知,步骤Ⅱ中发生的反应是铁与硫酸发生了反应,化学方程式为:Fe+H2SO4=FeSO4+H2↑.
(3)为了将硫酸亚铁和硫酸除去,步骤Ⅲ应进行的操作是加入适量的锌粉、过滤.
故答为:(1)有气泡产生,溶液由蓝色变为浅绿色;(2)Fe+H2SO4=FeSO4+H2↑;(3)加入适量的锌粉、过滤.
点评 本题考查了金属活动性顺序的应用,熟练掌握金属的活动性中排在氢前面的金属都可把酸中的氢置换出来而得到氢气;活动性强的金属可把活动性弱的金属从其盐溶液中置换出来是解题的关键.

| 植物汁液 | 酸性溶液 | 中性溶液 | 碱性溶液 |
| 紫甘蓝 | 红色 | 紫色 | 黄色 |
| 胡萝卜 | 橙色 | 橙色 | 橙色 |
| 月季花瓣 | 浅红色 | 红色 | 黄色 |
(2)将紫甘蓝的汁液滴加到pH约为2.5的柠檬汁中,溶液变成红色.

| A. | 牙膏 | B. | 胡萝卜 | C. | 西红柿 | D. | 食醋 |
 NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.
NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.查阅资料:(1)Ca(HCO3)2可溶于水
(2)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;Na2CO3的热稳定性好,受热不分解.
(3)不同温度下,Na2CO3、NaHCO3的溶解度如下表:
| 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 7.0g | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 6.9g | 8.1g | 9.6g | 11.1g | 12.7g |
| 设计者 实验步骤 | 1 | 2 | 3 |
| 小芳 | 加盐酸 | 溶解 | 加热 |
| 小明 | 溶解 | 加盐酸 | 加盐酸 |
| 小刚 | 溶解 | 加石灰水 | 加热 |
(2)小明和小刚的步骤1都是溶解,该步实验的目的是鉴别碳酸钙.
进行实验:小刚在进行步骤2时,发现在两只试管中产生了白色沉淀,小刚推测它们是Na2CO3、
NaHCO3.则NaHCO3与石灰水反应的产物可能是碳酸钠、碳酸钙和水.
反思与评价:(1)小刚的设计能不能完成鉴别,理由是不能,因为他的步骤2中碳酸钠和碳酸氢钠都产生的沉淀,步骤3的目的是将碳酸钠与碳酸氢钠区别开,碳酸氢钠加热会生成二氧化碳,碳酸钠不会.
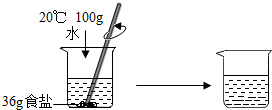
(2)小丽觉得大家的方案太麻烦,她跟老师要了一些氯化钠,做了如图所示的实验,由该实验得出的结论是20℃,100克水能溶解36克食盐.在此实验基础上,小芳用一步完成了鉴别,她的实验方法是取上述4种物质各25g,分别加入100克水溶解.
| A. | 质子数不同 | B. | 电子数不同 | ||
| C. | 中子数不同 | D. | 最外层电子数不同 |
下列表格中的叙述、对应的化学反应方程式和所属的反应类型都完全正确的是
选项 | 叙述 | 化学反应方程式 | 反应类型 |
A | 拉瓦锡研究空气成分 | 2HgO△2Hg+O2↑ | 分解反应 |
B | 探究一氧化碳的还原性 | CO + CuO△Cu + CO2 | 置换反应 |
C | 用二氧化碳制作碳酸饮料 | CO2+H2O=H2CO3 | 化和反应 |
D | 服用含氢氧化铝的药物 治疗胃酸过多 | Al(OH)3+3HCl= AlCl3+H2O | 复分解反应 |
A. A B. B C. C D. D