题目内容
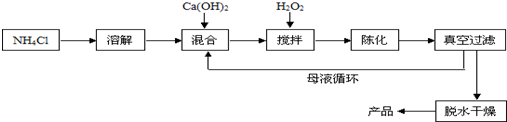
19.过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法.已知:温度过高过氧化钙会分解生成氧化物和氧气.方法1:由Ca(OH)2为原料最终制得,其制备流程如下:
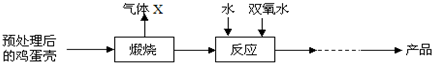
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如下:
(1)方法1中搅拌的目的是使反应充分,提高原料利用率.请将搅拌过程中发生反应的化学方程式补充完整:
CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl.制备过程中除水外可循环使用的物质是NH4C1(填化学式);
(2)方法2中气体X是CO2,实验室常用NaOH,溶液来吸收.煅烧后的反应时化合反应,也能生成CaO2•8H2O,反应的化学方程式为Ca(OH)2+H2O2+6H2O=CaO2•8H2O.该反应需控制温度在0~2℃,可将反应器放置在冰水中中,获得CaO2产品中主要含有的固体杂质是Ca(OH)2(填化学式);
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高除了防止氨水挥发外,还能使CaO2分解;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是方法2(填“方法1”或“方法2”).
分析 (1)根据搅拌可以使反应物充分混合进行分析,根据质量守恒定律进行分析,根据既是反应物也是生成物的物质可以循环利用进行分析;
(2)根据鸡蛋壳的主要成分是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以X是二氧化碳,在实验室常用氢氧化钠来吸收二氧化碳,氧化钙与水反应生成氢氧化钙,然后依据反应原理、质量守恒定律书写化学方程式,根据实验室控制温度的方法进行分析,根据题中的反应物进行分析;
(3)根据温度过高过氧化物会分解生成氧化物和氧气进行分析;
(4)根据绿色化学的条件进行分析.
解答 解:(1)搅拌可以使药品均匀混合,所以方法1中搅拌的目的是:使反应充分,提高原料利用率;依据质量守恒定律可知,化学反应前后原子个数不变,所以需要补充的物质是水,氯化铵既出现在了反应物中,也出现在了生成物中,所以制备过程中除水外可循环使用的物质是:NH4C1;
(2)鸡蛋壳的主要成分是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以X是二氧化碳,在实验室常用氢氧化钠来吸收二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙和双氧水反应生成过氧化钙晶体,化学方程式为:Ca(OH)2+H2O2+6H2O=CaO2•8H2O,冰水混合物的温度是0℃,所以反应需控制温度在0~2℃,可将反应器放置在冰水中,氢氧化钙是反应物,但是在反应过程中不一定会完全反应,所以获得的CaO2产品中主要含有的固体杂质是Ca(OH)2;
(3)依据题中的知识可知,温度过高过氧化物会分解生成氧化物和氧气,所以温度过高会造成氨水挥发外,还能使CaO2分解;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,方法2中没有副产物,方法1中有副产物二氧化碳,所以上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是:方法2.
故答案为:(1)使反应充分,提高原料利用率;H2O,NH4C1;
(2)CO2,NaOH,Ca(OH)2+H2O2+6H2O=CaO2•8H2O,冰水中,Ca(OH)2;
(3)使CaO2分解;
(4)方法2.
点评 在解此类题时,首先分析题中的反应流程,然后结合学过的知识和题中所给的知识进行分析解答.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 物质的制取和用途 | B. | 物质的变化和性质 | ||
| C. | 物体的运动状态 | D. | 物质的组成和结构 |
| A. | 生铁中含碳量比钢中含碳量小 | B. | 生铁中含有较多杂质 | ||
| C. | 四氧化三铁是生铁 | D. | 高炉炼出的是生铁生铁能用于炼钢 |
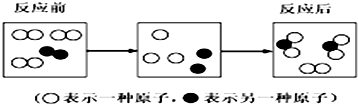

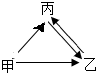 甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题:
甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题: