题目内容
5.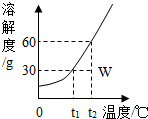 化合物W(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
化合物W(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )| A. | W的溶解度为60g | |
| B. | 将80gW溶液从t2℃降至t1℃析出W的质量为15g | |
| C. | t1℃时200g15%的W溶液蒸发掉60g水,溶液恰好达到饱和 | |
| D. | t2℃时,向50g水中加入40gW,得到溶液质量为80g |
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小;
根据物质的溶解度曲线、溶液质量可以判断析出溶质质量的多少;
饱和溶液和不饱和溶液之间可以相互转化;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液.
解答 解:A、t2℃时W的溶解度为60g,其他温度时溶解度不是60g,该选项说法不正确;
B、因为不知道溶液是否饱和,因此无法判断是否析出晶体及其晶体的质量,该选项说法不正确;
C、t1℃时200g15%的W溶液中含有30g溶质,溶剂质量是170g,蒸发掉60g水后溶剂是110g,110g水中溶解30g溶质时是不饱和溶液,该选项说法不正确;
D、t2℃时,溶解度是60g,向50g水中加入40gW时,只能够溶解30g,得到溶液质量是80g,该选项说法正确.
故选:D.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.环境问题是2015年我省主要工作之一,全省各地市都与省政府签下责令状,下列做法正确的是( )
| A. | 作物秸秆综合利用 | |
| B. | 野外焚烧工业垃圾 | |
| C. | 价高烟囱排放烟尘 | |
| D. | 为了减少雾霾天气,禁止使用私家车 |
20.碱石灰是NaOH与CaO的混合物,取一定量露置于空气中部分变质的碱石灰,加水充分搅拌后过滤,所得物质成分可能是( )
| 选项 | A | B | C | D |
| 滤液中的溶质 | NaOH、Na2CO3 | Na2CO3 | NaOH、Ca(OH)2 | NaOH |
| 滤渣 | CaCO3、Ca(OH)2 | CaCO3 | CaCO3、Ca(OH)2 | Ca(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
10.下列有关资源、能源和环境的叙述正确的是( )
| A. | 氧气约占空气总质量的21%,目前空气污染指数的项目有pM2.5、臭氧等 | |
| B. | 海洋中含量最多的元素是氧,可利用的陆地淡水只约占全球水储量的2.53% | |
| C. | 核能的利用可以减缓温室效应,石油可炼制出汽油、煤油和润滑油等产品 | |
| D. | 灯丝由熔点最高的金属钛制成,合金的强度和硬度一定比组成它的纯金属高 |
17.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )
| A. | KC1(KC1O3)--加二氧化锰,加热后冷却 | |
| B. | N2(O2)--通过灼热的铜网 | |
| C. | CO2(CO)--通过足量的氢氧化钠溶液 | |
| D. | KCl溶液(CaC12溶液)--滴加碳酸钠溶液至恰好完全反应,过滤 |
14.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,既可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,易分解生成HCl和一种常见的单质气体.HClO具有漂白性,能使品红等有色物质褪色.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如图1:
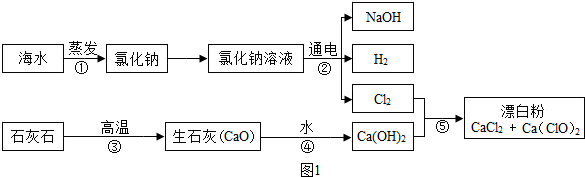
(1)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(2)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2 CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
【定量研究】
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.
【实验探究】
(3)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入如图2A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,计算过程中,保留3位小数,结果精确到0.1%)
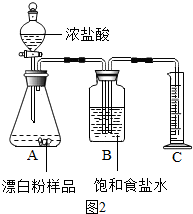
(4)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(5)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,易分解生成HCl和一种常见的单质气体.HClO具有漂白性,能使品红等有色物质褪色.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如图1:

(1)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(2)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2 CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加足量的稀盐酸. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 红色变浅或消失. |
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.
【实验探究】
(3)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入如图2A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,计算过程中,保留3位小数,结果精确到0.1%)

(4)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(5)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.

 目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要.
目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要.