题目内容
18.乙醇在空气中完全燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O点燃条件下,2.3g乙醇与4.0g氧气恰好完全反应,生成2.7g水,2.2g二氧化碳和一定质量的一氧化碳;则该反应的化学方程式为2C2H5OH+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2CO2+2CO,对比以上两个反应可知:反应物的量不同,生成物可能不同.分析 根据乙醇燃烧时能生成水和二氧化碳写出反应的化学方程式即可;根据质量守恒定律可知,反应前后物质的总质量不变,在化学反应前后原子个数不变,元素质量不变进行分析.
解答 解:乙醇在空气中完全燃烧能生成水和二氧化碳,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;根据2.3g乙醇与4.0g氧气恰好完全反应,生成2.7g水,2.2g二氧化碳和一定质量的一氧化碳可知,该反应的化学方程式为:2C2H5OH+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2CO2+2CO;
故答案为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;2C2H5OH+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2CO2+2CO.
点评 本题主要考查学生运用质量守恒定律进行推断的能力,难点在于结合化学式的计算确定物质的组成和书写化学方程式.

练习册系列答案
相关题目
8.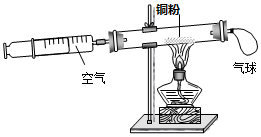 用如图所示装置来测定空气中氧气的含量,铜粉下列对该实验的认识中,错误的是( )
用如图所示装置来测定空气中氧气的含量,铜粉下列对该实验的认识中,错误的是( )
 用如图所示装置来测定空气中氧气的含量,铜粉下列对该实验的认识中,错误的是( )
用如图所示装置来测定空气中氧气的含量,铜粉下列对该实验的认识中,错误的是( )| A. | 铜粉用量的多少,会影响实验结果气球 空气 | |
| B. | 实验结束读数时,必须冷去至室温 | |
| C. | 气球的作用是调节气压,使氧气充分反应 | |
| D. | 操作无误的情况下,反应结束后消耗的氧 气体积约为反应前注射器中气体体积的$\frac{1}{5}$ |
9.如图所示物质的用途中,主要是利用其化学性质的是( )
| A. |  用石墨做干电池的电极 | B. |  用氢气做高能燃料 | ||
| C. |  用金刚石刀划破玻璃 | D. |  用铝做炊具 |
6.下列说法中不正确的是( )
| A. | 日常使用的金属材料,大多数属于合金 | |
| B. | 合金的性能一般比组成它的纯金属优越 | |
| C. | 灯泡里的灯丝用钨制是因为钨能导电且熔点高 | |
| D. | 金属都能与盐酸发生置换反应 |
3.下列变化中发生了化学变化的是( )
| A. | 石蜡熔化 | B. | 瓷碗破碎 | C. | 火柴燃烧 | D. | 胆矾研碎 |
7.在保持温度不变的条件下,蒸发掉氯化钠溶液中的部分水后,可能发生变化的是( )
| A. | 溶质的质量 | B. | 溶液的质量 | C. | 氯化钠的溶解度 | D. | 溶质的质量分数 |