题目内容
2.如图1是某学生用氯化钠(图中标示NaCl)固体和水配制500g、20%氯化钠溶液的部分操作过程,该同学在称量氯化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量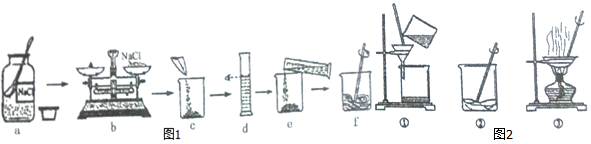
①该配制过程可归结为三步,依次为计算、称量、溶解.
②配置该溶液需要食盐为100克,水为400克.
③找出图中操作中的一处错误瓶塞正放、称量时左码右物.
④下列操作中导致溶质质量分数偏低的是AB(填字母).
A.b操作中砝码和氯化钠放错盘
B.c中烧杯用水洗涤后未干燥就使用
C.d操作中平视量筒凹液面最低处读数
D.e操作中有少量水溅出
⑤由于操作不规范,盛装氯化钠瓶子中混入了一些不溶于水的物质,该同学想提纯这些氯化钠,按照如图2进行实验,则:
(1)如图①,漏斗中的液面应低(填“高”或“低”)于滤纸边缘.
(2)如图②,玻璃棒的作用是搅拌,加速溶解.
(3)提纯时正确顺序是②①③(用序号填空)
分析 ①根据配制一定质量分数溶液的正确操作步骤是:计算、称量、溶解进行分析;
②根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量进行分析;
③根据瓶塞的方法和天平称量的注意事项进行分析;
④根据导致溶质质量分数偏低要从两个方面考虑:称量的溶质少了,量取的水多了进行分析;
⑤(1)根据过滤操作时,漏斗中的液面应低于滤纸边缘进行分析;
(2)根据在溶解过程中,玻璃棒的作用是:搅拌,加速溶解进行分析;
(3)根据提纯时正确顺序是:溶解、过滤、蒸发进行分析.
解答 解:①配制一定质量分数溶液的正确操作步骤是:计算、称量、溶解;
②配置该溶液需要食盐为:500g×20%=100克,水为500g-100g=400克;
③瓶塞应该倒放在桌面上,天平称量要左物右码;
④A、b操作中砝码和氯化钠放错盘,会导致称量氯化钠质量偏小,会导致溶质质量分数偏低,故A正确;
B、c中烧杯用水洗涤后未干燥就使用,会导致水多了,也会使溶质质量分数偏低,故B正确;
C、d平视量筒凹液面最低处读数,量取的水的量准确,溶质质量分数不会偏低,会准确,故C错误;
D、e操作中有少量水溅出,水少了会导致溶质质量分数偏大,故D错误;
故选:AB;
⑤(1)过滤操作时,漏斗中的液面应低于滤纸边缘;
(2)在溶解过程中,玻璃棒的作用是:搅拌,加速溶解;
(3)提纯时正确顺序是:溶解、过滤、蒸发,故选:②①③.
故答案为:①称量;
②100,400;
③瓶塞正放、称量时左码右物;
④AB;
⑤(1)低;
(2)搅拌,加速溶解;
(3)②①③.
点评 导致溶质质量分数偏低要从两个方面考虑:称量的溶质和量取的水进行分析,这是该题的难点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下面是对四个实验绘制的图形,其中实验结果与图形对应不正确的是( )
| A. | 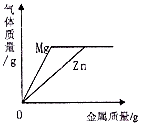 向两份完全相同的稀H2SO4中分别加入足量的锌粉、镁粉 | |
| B. | 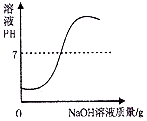 向一定量的稀盐酸中加入过量的NaOH溶液 | |
| C. | 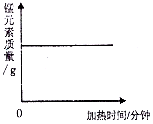 加热一定质量的KMnO4固体 | |
| D. | 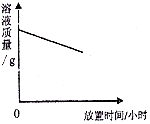 将一定量的浓H2SO4敞口放置在空气中 |
6.小林探究了影响物质溶解性的因素后.小林还认为:溶剂的多少也会影响物质溶解性.于是他进行相应的探究,请完成下列实验设计和问题交流.
【实验设计】
【问题交流】
(1)请你从控制变量角度优化步骤②向A烧杯倒入20克20℃的水,向B烧杯倒入60克20℃的水;
(2)步骤④需记录的是剩余食盐的质量;
(3)多次重复实验后,小林发现A、B两组在相同的条件下每10克水最多溶解食盐质量基本相同,于是得出结论:溶剂的多少不会影响物质溶解性.小红认为该实验还不具有普遍性.理由是加入水的质量相等.
【实验设计】
| 实验步骤 | 设计要求 |
| ①准备两个大小相同的烧杯,分别标为A、B;向两烧杯中分别倒入30克粗细相同的食盐. | 选择合适的实验器材 |
| ②向A烧杯倒入20克水,向B烧杯倒入60克水. | 设置对照实验 |
| ③都用玻璃棒充分搅拌直到A、B两烧杯底部的食盐不再溶解为止,过滤、干燥剩余食盐 | 控制实验条件 |
| ④称量并记录,并进行统计分析. | 观察和记录 |
(1)请你从控制变量角度优化步骤②向A烧杯倒入20克20℃的水,向B烧杯倒入60克20℃的水;
(2)步骤④需记录的是剩余食盐的质量;
(3)多次重复实验后,小林发现A、B两组在相同的条件下每10克水最多溶解食盐质量基本相同,于是得出结论:溶剂的多少不会影响物质溶解性.小红认为该实验还不具有普遍性.理由是加入水的质量相等.
7.某同学做实验时发现盛有NaOH溶液的试剂瓶口和橡胶塞上常有白色粉末出现.为了探究这种白色粉末的成分,设计如下实验,请你帮助完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 1、将白色粉末放于水中. | 白色粉末溶于水,形成无色溶液 | \ |
| 2、将无色酚酞滴入步骤1形成的无色溶液中. | 溶液颜色变红 | 该溶液呈碱性 |
| 3、在步骤2所形成的溶液中加入稀盐酸.并在试管口放一根燃烧的火柴. | 溶液由红色变成无色,燃烧的火柴熄灭了. | 溶液中含有碳酸根离子.白色粉末中含有氢氧化钠变质后生成的碳酸钠 |

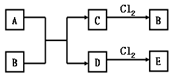 绝大多数金属都能与Cl2直接化合生成金属氯化物,如2Na+Cl2点燃═2NaCl,Cu+Cl2点燃═CuCl2等.已知A、B、C、D、E五种物质有如图转化关系(个别反应条件已略去).已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A、C都能与Cl2直接化合生成相应的金属氯化物B、E.回答下列问题:
绝大多数金属都能与Cl2直接化合生成金属氯化物,如2Na+Cl2点燃═2NaCl,Cu+Cl2点燃═CuCl2等.已知A、B、C、D、E五种物质有如图转化关系(个别反应条件已略去).已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A、C都能与Cl2直接化合生成相应的金属氯化物B、E.回答下列问题: