题目内容
2.从溶液中获得晶体方法有:降温结晶、蒸发结晶.海水中含有较多的氯化钠,要从海水中获得氯化钠固体,应采用上述哪种方法?不宜采用另一种方法的原因是什么?分析 根据冷却热饱和溶液结晶(降温结晶)一般适用于溶解度受温度影响变化较大的物质,如硝酸钾;蒸发溶剂结晶一般适用于溶解度受温度影响变化不大的物质,如氯化钠;进行分析解答.
解答 解:海水中含有较多的氯化钠,氯化钠的溶解度受温度的影响变化不大,要从海水中获得氯化钠固体,应采用蒸发结晶的方法.不能采用降温结晶的方法,因为氯化钠的溶解度受温度的影响变化不大,降低温度后,析出的晶体很少.
故答案为:蒸发结晶;氯化钠的溶解度受温度的影响变化不大,降低温度后,析出的晶体很少.
点评 本题难度不大,掌握结晶的原理、方法(降温结晶、蒸发结晶)并能灵活运用是正确解答本题的关键.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
13.两瓶无色溶液,一瓶是饱和食盐水,一瓶是蒸馏水,下面是某同学提供的几种鉴别方法:
①用光学显微镜观察;②用硝酸银溶液;③导电性实验;④用酚酞试液;⑤用生鸡蛋;⑥蒸发;⑦用石蕊试液.你认为可行的是( )
①用光学显微镜观察;②用硝酸银溶液;③导电性实验;④用酚酞试液;⑤用生鸡蛋;⑥蒸发;⑦用石蕊试液.你认为可行的是( )
| A. | ①②③⑤⑦ | B. | ②③⑤⑥ | C. | ①④⑤⑦ | D. | ②③⑤⑥⑦ |
17.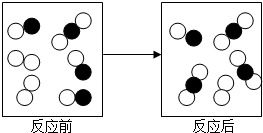 如图是某化学反应体系的微观模拟图,图中
如图是某化学反应体系的微观模拟图,图中 和
和 分别表示两种不同的原子,下列能用右图表示的化学反应是( )
分别表示两种不同的原子,下列能用右图表示的化学反应是( )
 如图是某化学反应体系的微观模拟图,图中
如图是某化学反应体系的微观模拟图,图中 和
和 分别表示两种不同的原子,下列能用右图表示的化学反应是( )
分别表示两种不同的原子,下列能用右图表示的化学反应是( )| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+CO2 |
7.下列现象都属于化学变化的是( )
①挥发;②蒸发;③破碎;④氧化;⑤燃烧;⑥液化;⑦还原;⑧蒸馏.
①挥发;②蒸发;③破碎;④氧化;⑤燃烧;⑥液化;⑦还原;⑧蒸馏.
| A. | ④⑤⑦ | B. | ④⑤⑥ | C. | ①②③ | D. | ①④⑧ |
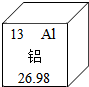 (1)铝是地壳中含量最多的金属元素,在元素周期 表中铝元素的信息如图所示:
(1)铝是地壳中含量最多的金属元素,在元素周期 表中铝元素的信息如图所示: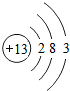 ;②铝离子的核外电子数为10;③工业上用电解熔融的方法冶炼铝,化学方程式为:2Al2O3$→_{冰晶石}^{通电}$4Al+3O2↑,该反应属于基本反应类型中的分解反应.
;②铝离子的核外电子数为10;③工业上用电解熔融的方法冶炼铝,化学方程式为:2Al2O3$→_{冰晶石}^{通电}$4Al+3O2↑,该反应属于基本反应类型中的分解反应.