题目内容
12.某化工厂生产的氧化亚铜(Cu2O)产品中常含有10%的金属铜.现准备用80t该氧化亚铜(Cu2O)产品生产10%的硫酸铜溶液.已知:Cu2O+H2SO4=CuSO4+Cu+H2O求:
(1)所需溶质质量分数20%的稀硫酸的质量;
(2)需要加水的质量.
分析 根据氧化亚铜的质量结合反应的化学方程式可以计算出硫酸的质量、生成的硫酸铜的质量以及铜的质量,然后根据溶液溶质的质量分数计算出所加水的质量即可.
解答 解:氧化亚铜的质量为:80t×(1-10%)=72t
设反应消耗H2SO4的质量是x,生成CuSO4的质量是y,Cu的质量为z.
Cu2O+H2SO4═CuSO4+Cu+H2O
144 98 160 64
72t x y z
$\frac{98}{x}$=$\frac{160}{y}$=$\frac{64}{z}$=$\frac{144}{72t}$
解得:x=49t y=80t z=32t
加入稀硫酸的质量=49t÷20%=245t
设加入水的质量为m
$\frac{80t}{72t+245t-32t+m}$×100%=10%
解得:m=515t
答:(1)需20%的稀硫酸249t,(2)加水的515t.
点评 根据化学反应方程式的计算的审题是非常关键的,一般是抓住“三找”;即一找化学反应方程式,二找已知量和未知量x,三找用到的相对质量关系

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
20.为验证甲、乙、丙三种金属的活动性顺序,把三种金属分别放入稀盐酸中,只有乙表面无明显变化,把甲放入丙的硝酸盐溶液中,甲的表面有丙析出,则甲、乙、丙三种金属的活动性顺序由强到弱的是( )
| A. | 丙 甲 乙 | B. | 甲 丙 乙 | C. | 乙 甲 丙 | D. | 丙 乙 甲 |
7.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观:水是由氢原子和氧原子构成的 | |
| B. | 根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化 | |
| C. | 根据结构观:氦原子和镁原子最外层电子数相同,化学性质相似 | |
| D. | 根据守恒观:10mL质量分数40%的硫酸,加l0mL水后质量分数变为20% |
2.下列有“水”字的物质中不属于纯净物的是( )
①冰水 ②硬水 ③海水 ④矿泉水 ⑤蒸馏水 ⑥雨水 ⑦苏打水.
①冰水 ②硬水 ③海水 ④矿泉水 ⑤蒸馏水 ⑥雨水 ⑦苏打水.
| A. | ①②④⑤⑥ | B. | ②③⑤⑥⑦ | C. | ③④⑤⑥⑦ | D. | ②③④⑥⑦ |
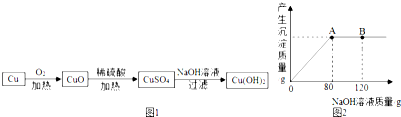
 已知A-F都是初中化学中常见的物质,其中A和C是无色无味气体,B是红色固体,D是黑色粉末,它们的转化关系如图所示.(部分生成物已省略)
已知A-F都是初中化学中常见的物质,其中A和C是无色无味气体,B是红色固体,D是黑色粉末,它们的转化关系如图所示.(部分生成物已省略)