题目内容
8.生石灰(化学式为CaO)样品中常含有少量的杂质碳酸钙(CaCO3).为了测定该生石灰样品中生石灰的质量分数,进行如下实验:取该生石灰样品6.6g,对其进行高温煅烧,充分反应后的剩余固体6.16g.计算:(1)生石灰样品中生石灰的质量分数.
(2)该样品中钙元素的质量分数.(计算结果精确到0.1%)
分析 (1)碳酸钙受热分解生成氧化钙和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算生石灰样品中生石灰的质量分数;
(2)根据生石灰样品中生石灰的质量和碳酸钙的质量,进一步可以计算该样品中钙元素的质量分数.
解答 解:(1)生成二氧化碳质量为:6.6g-6.16g=0.44g,
设碳酸钙的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
100 44
x 0.44g
则$\frac{100}{44}=\frac{x}{0.44g}$,解得x=1g,
生石灰样品中生石灰的质量分数为:$\frac{6.6g-1g}{6.6g}$×100%≈84.8%,
(2)该样品中钙元素的质量分数:$\frac{6.16g×\frac{40}{56}×100%}{6.6g}$×100%≈66.7%.
故答案为:(1)84.8%;(2)66.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
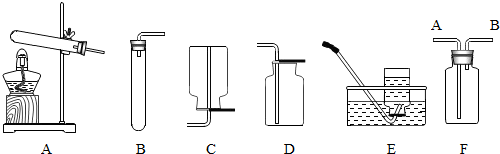
18.如图所示的实验操作不正确的是( )
| A. | 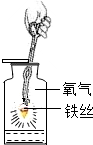 铁丝在氧气中的燃烧 | B. |  检验空气中氧气含量 | ||
| C. |  探究分子不断运动 | D. |  溶液滴定 |
19.下列关于分子和原子的说法,正确的是( )
| A. | 在化学变化中分子可以再分、原子不可以再分 | |
| B. | 分子不停地运动,原子静止不动 | |
| C. | 在化学反应前后,分子和原子的种类保持不变 | |
| D. | 不同种类的原子,不能相互结合成分子 |
6.符合以下四位同不所描述的化学式可能是( )
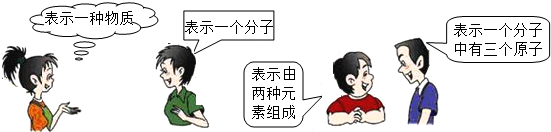

| A. | CO2 | B. | O2 | C. | MgO | D. | HClO |
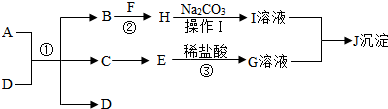 下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答:
下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答: