题目内容
12.甲、乙、丙三位同学为一家化工厂的污水设计排污方案,请你就他们的探究过程回答有关问题.Ⅰ.首先用pH试纸检测污水的酸碱性.三位同学分别进行如下实验:
甲:取pH试纸于玻璃片上,用玻璃棒蘸取待测液滴在pH试纸行,测得pH<7;
乙:取pH试纸于玻璃片上,先用蒸馏水湿润,再用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7;
丙:取pH试纸直接浸入待测液中,测得pH<7.
(1)以上三位同学中操作规范的是甲,污水显酸.
Ⅱ.利用中和反应原理测定污水中污染物(设为盐酸)的质量分数.
甲、乙两同学设计的方案如图甲、乙所示:

(2)甲同学取少量反应后的溶液于试管中,滴加几滴无色酚酞试液,酚酞变红色,于是得出“两种物质已恰好中和”的结论.你认为他的结论是否正确?不正确;,理由是氢氧化钠溶液过量使酚酞试液变成红色.
(3)乙同学当观察到溶液由红色变成紫色现象时即恰好完全反应,若此时消耗NaOH溶液2g,则污水中HCl的质量分数为0.00365%.
(4)实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且要用玻璃棒不断搅拌,目的是防止氢氧化钠过量,使反应充分进行.
(5)除去污水中的盐酸,你建议选用的原料是B.
A.NaOH;B.Ca(OH)2;C.CuO;D.Fe.
分析 (1)根据PH值的正确测定方法来考虑,否则测得的结果会产生误差;根据pH和溶液酸碱性的关系分析;
(2)根据酚酞试液在碱性溶液为红色分析结论的正确性;
(3)根据紫色石蕊试液在酸性、碱性、中性溶液中的颜色分析反应的程度并通过化学方程式进行计算;
(4)根据实验的注意事项分析玻璃棒的作用;
(5)根据酸的性质及可操作性、经济性等分析
解答 解:(1)测PH值的正确测定方法是:取pH试纸放在玻璃片上,用玻璃棒蘸取待测溶液沾在pH试纸上,将试纸显示的颜色与标准比色卡比较,即可得到PH值,所以乙同学、丙同学操作都是错误的,用蒸馏水将pH试纸润湿再测该酸性溶液PH值,结果会偏大;将pH试纸直接浸入溶液中会污染试剂;测得废水的pH<7,说明显酸性;
(2)根据取少量反应后的溶液于试管中,滴加几滴无色酚酞试液,酚酞变红色,说明此时的溶液显碱性,是因为氢氧化钠溶液过量;
(3)石蕊试液在酸性废水中出现红色,当滴加氢氧化钠的过程中,当溶液由红色变成紫色时恰好完全反应;
设污水中HCl的质量分数为x,
HCl+NaOH=NaCl+H2O
36.5 40
20gx 2g×0.04%
$\frac{36.5}{20gx}=\frac{40}{2g×0.04%}$
x=0.00365%
所以污水中HCl的质量分数为0.00365%;
(4)为了防止氢氧化钠过量,使反应充分进行,实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且要用玻璃棒不断搅拌;
(5)A.NaOH;B.Ca(OH)2;C.CuO;D.Fe四种物质都能够和盐酸发生反应,但从经济的角度考虑,氢氧化钙最便宜,所以选择B;
故答案为:(1)甲;酸;(2)不正确;氢氧化钠溶液过量使酚酞试液变成红色;(3)溶液由红色变成紫色;0.00365%;(4)防止氢氧化钠过量,使反应充分进行;(5)B.
点评 本题考查了酸碱度的测定方法的评价,酸碱性与pH的关系以及酸碱中和反应的运用等,综合性较强,但难度不大,关键还是熟练掌握溶液酸碱性、酸碱度测定的方法及酸碱中和反应的原理.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案| A. | 镁在空气中燃烧生成氧化镁 | |
| B. | 一氧化碳还原氧化铁实验中固体颜色由黑变红 | |
| C. | 硫在氧气中燃烧发出蓝紫色火焰 | |
| D. | 白磷在空气中燃烧产生大量白雾 |
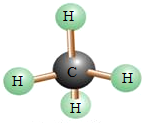
| A. | 该物质属于化合物 | B. | 该物质的化学式为CH4 | ||
| C. | 该物质的1个分子中含有5个原子 | D. | 该物质中碳、氢元素质量比为1:4 |
| A. | 葡萄酿酒 | B. | 榨取果汁 | C. | 米饭变馊 | D. | 蛋清受热凝固 |
| A. | 冰雪融化 | B. | 食物腐烂 | C. | 酒精挥发 | D. | 干冰升华 |
| 现象 | 解释 | |
| A | 打开啤酒瓶盖,有大量气体冒出 | 压强减小,气体溶解度减小 |
| B | 走进花园,闻到花香 | 分子在不停的运动 |
| C | 把50mL水和50mL酒精混合后总体积小于100mL | 分子间有间隔 |
| D | 温度计中的水银(汞)热胀冷缩 | 原子的大小发生了变化 |
| A. | A | B. | B | C. | C | D. | D |
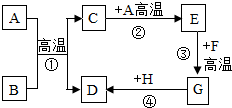 初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色溶液.它们的转化关系如图所示.请回答:
初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色溶液.它们的转化关系如图所示.请回答: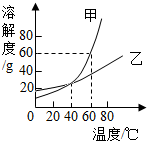 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题: