题目内容
18.已知含Ba2+的溶液会使人中毒,透视时通常服用“钡餐”,其成分是BaSO4而不能用BaCO3,这是由于BaCO3+2HCl=BaCl2+H2O+CO2↑(填化学方程式),若误服,应立即服泻盐MgSO4,其理由是(填化学方程式)BaCl2+MgSO4=BaSO4↓+MgCl2.分析 根据题意,含Ba2+的溶液会使人中毒,透视时通常服用“钡餐”,其成分是BaSO4而不能用BaCO3,人体胃液中含有一定量盐酸,盐酸能与碳酸钡反应生成氯化钡、水和二氧化碳,要想解毒,应将可溶性钡盐转化为不溶性性钡盐,据此进行分析解答.
解答 解:含Ba2+的溶液会使人中毒,透视时通常服用“钡餐”,其成分是BaSO4而不能用BaCO3,人体胃液中含有一定量盐酸,盐酸能与碳酸钡反应生成氯化钡、水和二氧化碳,反应的化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑.
若误服,应立即服泻盐MgSO4,MgSO4能与氯化钡反应生成既不溶于水也不溶于酸的硫酸钡沉淀,反应的化学方程式为:BaCl2+MgSO4=BaSO4↓+MgCl2.
故答案为:BaCO3+2HCl=BaCl2+H2O+CO2↑;BaCl2+MgSO4=BaSO4↓+MgCl2.
点评 本题难度不大,灵活运用盐的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
8.向硝酸银、硝酸铜的混合溶液中加入一些铁粉,等完全反应后再过滤.下列情况不可能出现的是( )
| A. | 滤纸上若有Ag,滤液中可能有有Fe2+、Cu2+、Ag+ | |
| B. | 滤纸上若有Ag、Cu,滤液中不可能有Ag+ | |
| C. | 滤纸上若有Ag、Cu、Fe,滤液中一定只有Fe2+ | |
| D. | 滤纸上若有Ag、Cu、Fe,滤液中可能有Cu2+、Ag+ |
13.对某物质的饱和溶液描述正确的是( )
| A. | 在100g水里不能再溶解该物质的溶液 | |
| B. | 在t℃时,不能再溶解该物质的溶液 | |
| C. | 在t℃时,在一定量的溶剂里不能再溶解该物质的溶液 | |
| D. | 在条件不变时,保持稳定的该物质的溶液 |
10. 小军以木条为基本原料,进行了如下一系列探究实验:
小军以木条为基本原料,进行了如下一系列探究实验:
(1)对木条组成的探究:
(2)小军根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木条燃烧产生的木炭代替红磷测定空气中氧气的含量,并按如图装置进行实验.
①依据的实验原理是木炭燃烧消耗氧气
小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象.
经过认真分析,小军发现实验失败的原因是(答一条)木炭燃烧虽消耗了氧气,但产生了新的气体,致使集气瓶内气体压强未减少
②小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)药品要在空气中燃烧.
 小军以木条为基本原料,进行了如下一系列探究实验:
小军以木条为基本原料,进行了如下一系列探究实验:(1)对木条组成的探究:
| 实验操作 | 实验现象 | 实验结论 | 方法提炼 |
| 点燃干燥的木条,在火焰上方罩一干燥的冷烧杯 | 一会儿烧杯内壁有水雾产生. | 木条中一定含有氢元素 | 根据实验现象 可以推测出实验结论. |
| 继续把火焰靠近烧杯底部 | 一会儿烧杯底部出现一层黑色物质 | 木条中一定含有碳元素 |
①依据的实验原理是木炭燃烧消耗氧气
小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象.
经过认真分析,小军发现实验失败的原因是(答一条)木炭燃烧虽消耗了氧气,但产生了新的气体,致使集气瓶内气体压强未减少
②小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)药品要在空气中燃烧.
8.向硝酸银、硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中滴加稀盐酸有白色沉淀产生,下列说法正确的是( )
| A. | 所得滤液中可能含有Cu2+ | |
| B. | 所得滤渣中可能含有Cu | |
| C. | 所得滤液中一定含有Ag+、Cu2+、Fe2+ | |
| D. | 所得滤渣中一定含有Ag和Cu |

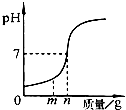 用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.
用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.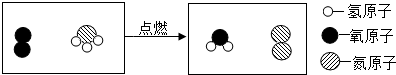 研究发现NH3燃烧能释放大量的能量,有一定的应用前景.其反应的微观示意图如图所示:
研究发现NH3燃烧能释放大量的能量,有一定的应用前景.其反应的微观示意图如图所示: