题目内容
13.碳酸钡广泛应用于显像管、光学玻璃等行业.有一种碳酸盐矿石,其主要成分是碳酸钙和碳酸钡.现有该碳酸盐矿石粉末样品(假设杂质不溶于水,也不与盐酸反应),为检验该样品的主要成分,小明同学做了一个实验:取少量样品于烧杯中,加入过量的稀盐酸.(1)在小明同学的实验中,可观察到的实验现象是固体部分溶解,产生气泡,该实验的目的是检验样品中含有碳酸盐.
(2)在小明同学实验的基础上,请你设计一个实验方案,以进一步证明该碳酸盐矿石的主要成分是碳酸钙和碳酸钡.(本实验条件下,微溶物不形成沉淀)
| 实验操作 | 预期现象与结论 |
| 取小明同学实验中的少量滤液于烧杯中,向烧杯中 加入过量的稀硫酸,并用玻璃棒搅拌. | 有白色沉淀生成,说明含有硫酸根离子,证明矿石中含有碳酸钡 |
| 向上述实验中的上层清液加入足量的碳酸钠溶液 | 有白色沉淀生成,说明含有钙离子,证明矿石中含有碳酸钙 |
分析 根据碳酸盐遇酸化气的知识进行分析解答,要证明含有碳酸钙和碳酸钡,就是证明钙离子和钡离子的存在,据此解答.
解答 解:(1)碳酸盐加入盐酸,则含有的碳酸根离子能与酸反应产生二氧化碳气体,其中的杂质不会溶解,故会观察到有气泡产生,故填:固体部分溶解,产生气泡;检验样品中含有碳酸盐;
(2)要证明含有的矿石的主要成分是碳酸钙和碳酸钡,就是证明钙离子和钡离子的存在,由于钡离子与硫酸根离子形成的硫酸钡不溶于水,而钙离子与硫酸根离子的形成的硫酸钙是微溶于水的,不会形成沉淀,故可以加入过量的硫酸检验并且除去钡离子,检验钙离子存在,可以加入足量的碳酸钠溶液,最终观察到有沉淀生成,故填:过量的稀硫酸;有白色沉淀生成,说明含有硫酸根离子,证明矿石中含有碳酸钡;向上述实验中的上层清液加入足量的碳酸钠溶液;有白色沉淀生成,说明含有钙离子,证明矿石中含有碳酸钙.
点评 本题考查的是常见的离子检验,完成此题,可以依据已有的物质的性质以及物质的溶解性进行.

练习册系列答案
相关题目
1.配制一定质量分数的食盐溶液时,会引起食盐质量分数偏小的操作是( )
| A. | 称量固体食盐时,所用砝码已生锈 | |
| B. | 称量完固体食盐时,天平指针向左倾斜 | |
| C. | 用量筒取水时,仰视读数 | |
| D. | 取已配制好的食盐溶液时,有少量溶液洒在瓶外 |
8.在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是 ( )
| A. | 滤液中一定有Fe(NO3)3 和Zn(NO3)2 | B. | 滤渣中一定有Ag、Cu、Fe和Zn | ||
| C. | 滤渣中只有Ag和Cu,一定无Zn | D. | 滤渣中一定有Ag、Cu和Fe,一定无Zn |
18.下列四个有关燃烧的实验解释错误的是( )
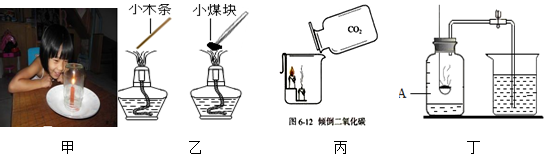

| A. | 甲图实验中,瓶内的蜡烛燃烧一会儿就熄灭了,说明燃烧需要氧气 | |
| B. | 乙图中,小木条马上被点燃,小煤块点不燃,是因为煤块的着火点比较高 | |
| C. | 丙图实验中,蜡烛火焰自下而上熄灭,说明CO2密度比空气大 | |
| D. | 丁图测量空气中的氧气含量实验,把燃烧匙内红磷换成木炭效果会更好 |
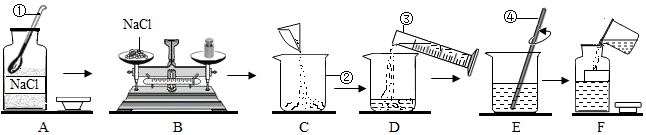
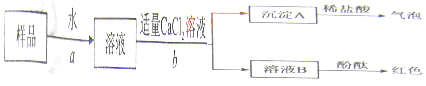
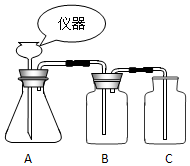 根据如图装置回答下列问题:
根据如图装置回答下列问题: