题目内容
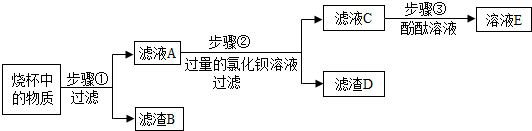
6.实验室去除粗盐中难溶性杂质的过程如图所示.
①步骤①中使用玻璃棒的目的是加速溶解.
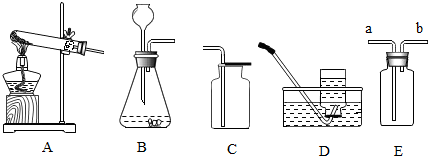
②步骤②中过滤器的制作如图2,正确的顺序是CAB(填序号).
③步骤③的名称是蒸发,当观察到出现较多固体时,停止加热.
分析 ①步骤①中使用玻璃棒的目的是加速溶解;
②步骤②中过滤器的制作如图2,正确的顺序是CAB;
③步骤③的名称是蒸发,当观察到出现较多固体时,停止加热.
解答 解:①步骤①中使用玻璃棒的目的是加速溶解.
故填:加速溶解.
②步骤②中过滤器的制作如图2,正确的顺序是CAB.
故填:CAB.
③步骤③的名称是蒸发,当观察到出现较多固体时,停止加热.
故填:蒸发;出现较多固体.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.除去粗盐中难溶性杂质并计算产率的实验中,下列实验操作正确的是( )
| A. |  溶解 | B. |  过滤 | C. |  蒸发 | D. |  称量并计算 |
1.小明同学欲回收中考化学实验操作考试(考题:鉴别碳酸钠和氯化钠两瓶白色固体)用剩的药品.他对其中的一瓶药品是否纯净产生质疑,于是他在老师的指导下对其成分展开可如下探究:
【猜想与假设】猜想一:白色固体为碳酸钠;
猜想二:白色固体为氯化钠;
猜想三:白色固体为碳酸钠和氯化钠的混合物.
【设计与实验】
【实验结论】小明同学根据实验现象得出猜想三正确.
【反思评价】小明同学根据实验结论领悟到:老师强调加入稀硝酸并且至过量的目的是检验碳酸钠的存在并将碳酸钠除掉.他认为,若只将实验步骤中的过量稀硝酸换成过量稀盐酸,重复以上实验操作,虽然也会产生相同的实验现象,但不能确认猜想三是否正确,理由是盐酸与碳酸钠反应生成了新的氯化钠,就不能确定,加入硝酸银产生的沉淀,是原来的氯化钠与硝酸银产生的,还是盐酸与碳酸钠反应生成的氯化钠与硝酸银反应生成的;.
【归纳总结】1.在选加试剂检验物质成分时,既要考虑除尽原有的干扰物质,又要防止引入新的干扰物质.
2.在实验操作过程中,应规范操作以避免药品被污染.
【猜想与假设】猜想一:白色固体为碳酸钠;
猜想二:白色固体为氯化钠;
猜想三:白色固体为碳酸钠和氯化钠的混合物.
【设计与实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量固体药品,装入试管,加蒸馏水溶解,然后加入过量的稀硝酸,最后滴加几滴硝酸银溶液 | 若只有气泡产生产生 | 则猜想一正确 |
| 若只有白色沉淀生成 | 则猜想二正确 反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3 | |
| 若先有气泡产生,后有白色沉淀生成 | 则猜想三正确 |
【反思评价】小明同学根据实验结论领悟到:老师强调加入稀硝酸并且至过量的目的是检验碳酸钠的存在并将碳酸钠除掉.他认为,若只将实验步骤中的过量稀硝酸换成过量稀盐酸,重复以上实验操作,虽然也会产生相同的实验现象,但不能确认猜想三是否正确,理由是盐酸与碳酸钠反应生成了新的氯化钠,就不能确定,加入硝酸银产生的沉淀,是原来的氯化钠与硝酸银产生的,还是盐酸与碳酸钠反应生成的氯化钠与硝酸银反应生成的;.
【归纳总结】1.在选加试剂检验物质成分时,既要考虑除尽原有的干扰物质,又要防止引入新的干扰物质.
2.在实验操作过程中,应规范操作以避免药品被污染.
18.“低碳生活”目前已成为一种生活态度和时尚,指的是生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化,下列行为中不符合“低碳生活”的精神的是( )
| A. | 避免购买不需要的物品,少穿化纤材质的服装 | |
| B. | 推广无纸化办公,使用再生纸且双面打印文印 | |
| C. | 夏天将空调开的很低 | |
| D. | 使用手绢代替餐巾纸 |
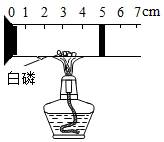 我们已经知道空气的主要成分是氮气和氧气,如图所示为测定 空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以活动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,试验开始前活塞处在刻度5cm处.请按要求填空.
我们已经知道空气的主要成分是氮气和氧气,如图所示为测定 空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以活动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,试验开始前活塞处在刻度5cm处.请按要求填空.