题目内容
9.某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石.图 1 是利用该镁矿石制备七水硫酸镁(MgSO4•7H2O)的工艺 流程:
已知 CaSO4 和 MgSO4 的溶解度曲线如图 2 所示:
根据以上信息回答下列问题:
(1)写出步骤①中发生反应的化学方程式MgCO3+H2SO4═MgSO4+H2O+CO2↑或CaCO3+H2SO4═CaSO4+H2O+CO2↑(任写一个).
(2)上述流程中多次用到了过滤操作,实验室过滤时需要用到的玻璃仪器是玻璃棒、烧杯和漏斗.
(3)沉淀 A 的成分是 SiO2和部分硫酸钙,过滤Ⅰ后得到的滤液中的溶质除了MgSO4还有CaSO4.
(4)步骤④趁热过滤的目的是MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶.
(5)步骤⑦的操作名称是过滤.
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)由于煤矿石主要成分为碳酸镁,还含有较多的脉石(SiO2)和少量石灰石,加入硫酸时,碳酸镁和碳酸钙都和硫酸反应,生成对应的硫酸盐和水以及二氧化碳,对应的化学方程式为MgCO3+H2SO4═MgSO4+H2O+CO2↑ 或CaCO3+H2SO4═CaSO4+H2O+CO2↑(任写一个).
(2)上述流程中多次用到了过滤操作,实验室过滤时需要用到的玻璃仪器是玻璃棒、烧杯和漏斗.
(3)沉淀 A 的成分是 SiO2和部分硫酸钙,所以得到的滤液应该是硫酸钙的饱和溶液,因此过滤Ⅰ后得到的滤液中的溶质除了MgSO4还有 CaSO4.
(4)步骤④趁热过滤的目的是 MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶.
(5)步骤⑦是将晶体分离出来,是固体和液体的分离,为过滤.
故答案为:
(1)MgCO3+H2SO4═MgSO4+H2O+CO2↑ 或CaCO3+H2SO4═CaSO4+H2O+CO2↑;
(2)漏斗;
(3)CaSO4;
(4)MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶;
(5)过滤.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
20.PM2.5是指大气中直径小于或等于2.5微米的可吸入颗粒物,PM2.5对人体健康危害极大.下列措施不会影响大气中PM2.5浓度的是( )
| A. | 合理密植灌木,提高城市的绿化面积 | |
| B. | 报废超排车辆,提高机动车燃油的质量 | |
| C. | 为减少垃圾的占地及污染,将可燃垃圾露天焚烧掉 | |
| D. | 雾霾天尽量减少室外活动 |
17.下列说法中不正确的是( )
| A. | 纯碱是发酵粉的主要成分 | B. | 硫酸可用于制铅酸蓄电池 | ||
| C. | 烧碱可用于生产炉具清洁剂 | D. | 熟石灰可用于改良酸性土壤 |
10.下列氯化镁的化学式书写正确的是( )
| A. | MgCl2 | B. | MgCL2 | C. | MgCl | D. | MgAl |
 青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯.
青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯.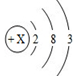 是铝的原子结构示意图,则X=13,铝原子在化学变化中容易形
是铝的原子结构示意图,则X=13,铝原子在化学变化中容易形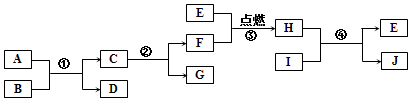
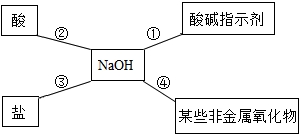
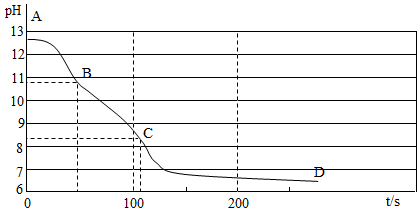
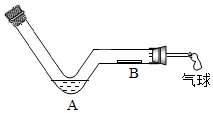 如图所示
如图所示