��Ŀ����
��ѧ��ȤС���ijʯ��ʯ��Ʒ��̼��Ƶĺ�������ʵ��̽������С��ȡ��4g��Ʒ���ⶨ��ʯ��ʯ�Ĵ��ȣ���δ֪��������������ϡ����40g��4�μ��롣ÿ�γ�ַ�Ӧ�����ˡ�����Ȳ���������������������������ˡ�����Ȳ������̣��������ʵ�����������ģ�ʯ��ʯ�е����ʲ������ᷴӦ��Ҳ������ˮ����ʵ�������±���

����㣺
(1) ��ʯ��ʯ��Ʒ��̼��Ƶ����������Ƕ��٣�
(2) ���õ�ϡ�����У����ʵ����������Ƕ��٣�
(3) 4gʯ��ʯ��Ʒ��������ϡ���ᷴӦ�����ɶ�����̼���ٿˣ�
(1) ��ʯ��ʯ��Ʒ��̼��Ƶ����������Ƕ��٣�
(2) ���õ�ϡ�����У����ʵ����������Ƕ��٣�
(3) 4gʯ��ʯ��Ʒ��������ϡ���ᷴӦ�����ɶ�����̼���ٿˣ�
��1��ʯ��ʯ��Ʒ��CaCO3����������Ϊ��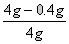 =90%
=90%
��2���⣺���һ��ʵ���У��������10g���������ʵ�����Ϊx
CaCO3+2HCl===CaCl2+H2O+CO2��
100 73
1g x
100 ��73 = 1g ��x x=0.73g
ϡ���������ʵ���������=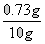 ��100%=7.3%
��100%=7.3%
��3���⣺���ʵ�����ɶ�����̼������Ϊy
CaCO3+2HCl===CaCl2+H2O+CO2��
100 44
3.6g y
100 ��44 =3.6g ��y y=1.6g
��ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ90%��ϡ���������ʵ���������Ϊ7.3%������4gʯ��ʯ��Ʒ���ɶ�����̼1.6g��
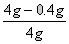 =90%
=90%��2���⣺���һ��ʵ���У��������10g���������ʵ�����Ϊx
CaCO3+2HCl===CaCl2+H2O+CO2��
100 73
1g x
100 ��73 = 1g ��x x=0.73g
ϡ���������ʵ���������=
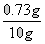 ��100%=7.3%
��100%=7.3%��3���⣺���ʵ�����ɶ�����̼������Ϊy
CaCO3+2HCl===CaCl2+H2O+CO2��
100 44
3.6g y
100 ��44 =3.6g ��y y=1.6g
��ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ90%��ϡ���������ʵ���������Ϊ7.3%������4gʯ��ʯ��Ʒ���ɶ�����̼1.6g��

��ϰ��ϵ�д�
�����Ŀ
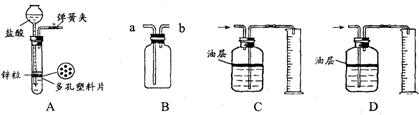
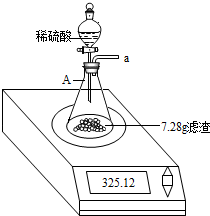 һ��ѧ��ȤС���ij�±���װ���еġ����������ܺ��棬���ǹ۲쵽�������������װ��ע�ijɷ�Ϊ���ۡ�����̿���Ȼ��ƣ����ֻҺ�ɫ�Ĺ����л���������������ɫ��ĩ��
һ��ѧ��ȤС���ij�±���װ���еġ����������ܺ��棬���ǹ۲쵽�������������װ��ע�ijɷ�Ϊ���ۡ�����̿���Ȼ��ƣ����ֻҺ�ɫ�Ĺ����л���������������ɫ��ĩ��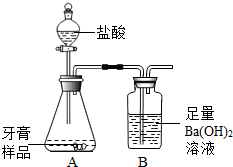 ��2013?�����ж�ģ����ѧ��ȤС���ijƷ��������̼��ƺ�����������̽����������Ħ������Ҫ��̼��ơ�����������ɣ������ɷ���������ʱ���������ɣ���������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨB�����ɵ�BaCO3������������ȷ��̼��Ƶ�������������ش��������⣮
��2013?�����ж�ģ����ѧ��ȤС���ijƷ��������̼��ƺ�����������̽����������Ħ������Ҫ��̼��ơ�����������ɣ������ɷ���������ʱ���������ɣ���������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨB�����ɵ�BaCO3������������ȷ��̼��Ƶ�������������ش��������⣮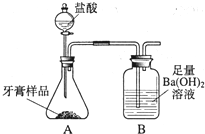 ��ѧ��ȤС���ijƷ��������̼��ƺ�����������̽����������Ħ������Ҫ��̼��ơ�����������ɣ������ɷ���������ʱ���������ɣ���������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨB�����ɵ�BaCO3������������ȷ��̼��Ƶ�������������ش��������⣮
��ѧ��ȤС���ijƷ��������̼��ƺ�����������̽����������Ħ������Ҫ��̼��ơ�����������ɣ������ɷ���������ʱ���������ɣ���������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨB�����ɵ�BaCO3������������ȷ��̼��Ƶ�������������ش��������⣮ һ��ѧ��ȤС���ij�±���װ���еġ����������ܺ��棬���ǹ۲쵽�������������װ��ע�ijɷ�Ϊ���ۡ�����̿���Ȼ��ƣ����ֻҺ�ɫ�Ĺ����л���������������ɫ��ĩ��
һ��ѧ��ȤС���ij�±���װ���еġ����������ܺ��棬���ǹ۲쵽�������������װ��ע�ijɷ�Ϊ���ۡ�����̿���Ȼ��ƣ����ֻҺ�ɫ�Ĺ����л���������������ɫ��ĩ��