题目内容
6.硫酸亚铁铁(FeSO4)可用于治疗缺铁性贫血,根据硫酸亚铁的化学式计算:(要求写出计算过程):求(1)铁元素的化合价以及硫酸亚铁中铁、硫、氧三种元素的质量比.
(2)硫酸亚铁中铁元素的质量分数.
分析 (1)根据化合物中正负总数和为0、或化合物的读法计算铁元素的化合价,并据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答
解答 解:(1)硫酸亚铁中硫酸根的化合价是-2价,据化合物中正负总数和为0可知铁元素的化合价是+2价,或据其读法推测,铁有两个化合价:+2、+3,低价态的铁元素形成的化合物读:亚铁,所以硫酸亚铁中铁元素显+2价;
硫酸亚铁中铁、硫、氧三种元素的质量比56:32:(16×4)=7:4:8.
(2)硫酸亚铁中铁元素的质量分数=$\frac{56}{56+32+16×4}$×100%≈36.8%;
故答案为:(1)铁元素的化合价是+2,硫酸亚铁中铁、硫、氧三种元素的质量比是7:4:8;
(2)硫酸亚铁中铁元素的质量分数36.8%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
16.某学校在探究铝的化学性质时,实验情况如下:
[提出问题]:铝片放入稀硫酸中,开始时为什么没有明显现象?
[提出假设]:假设1:铝片表面有致密的氧化膜阻碍了反应的进行
假设2:所用稀硫酸的浓度太小
假设3:铝片与稀硫酸反应需要加热
[实验设计]:
你选择的假设是1或2或3.请选择恰当的实验用品进行实验,
证明假设成立.
有以下实验用品:大小相同的铝片、l0%的稀硫酸、30%的稀硫酸、氯化钠、
试管、试管夹、酒精灯、镊子、药匙、砂纸
[评价与反思]:通过这次探究,你从中得到的启示是:善于发现问题,大胆质疑,勇于探究.
| 实验操作 | 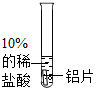 |
| 实验现象 | 开始时.铝片表面没有明显现象 |
[提出假设]:假设1:铝片表面有致密的氧化膜阻碍了反应的进行
假设2:所用稀硫酸的浓度太小
假设3:铝片与稀硫酸反应需要加热
[实验设计]:
你选择的假设是1或2或3.请选择恰当的实验用品进行实验,
证明假设成立.
有以下实验用品:大小相同的铝片、l0%的稀硫酸、30%的稀硫酸、氯化钠、
试管、试管夹、酒精灯、镊子、药匙、砂纸
| 实验步骤(文字叙述或图示可) | 观察到的现象 | 结论 |
| 假设成立 |
16.成语”釜底抽薪“的本意包含着灭火的原理.下列灭火方法也依据这个原理的是( )
| A. | 消防队员用高压水枪灭火 | B. | 用液态二氧化碳灭火器灭火 | ||
| C. | 用锅盖盖灭着火的油锅 | D. | 砍掉树木形成隔离带 |
 假期生活丰富多彩,某校组织同学们夏令营活动.
假期生活丰富多彩,某校组织同学们夏令营活动.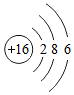 表示S的原子结构示意图.
表示S的原子结构示意图.