题目内容
4.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.Ⅰ.写出该中和反应的化学方程式:Ca(OH)2+2HCl=CaCl2+2H2O.
Ⅱ.探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡
实验现象:溶液无明显变化(或溶液不变红色),结论:猜想一不正确
实验步骤:实验步骤取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
实验现象:先有气体产生,后产生沉淀,结论:猜想二不正确,猜想三正确
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?ac(填序号)
a.pH试纸 b.铜 c.紫色石蕊溶液 d.硝酸银溶液
(3)要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的碳酸钙.
分析 I、根据氢氧化钙和盐酸反应生成氯化钙和水进行分析;
【猜想】根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余进行分析;
【进行实验】根据酚酞遇碱变红,在中性和碱性环境中不变色来进行解答;
【反思与拓展】(1)根据实验的结论进行反思;
(2)根据盐酸的化学性质和氯化钙中也含有氯离子进行分析;
(3)根据除杂的原则进行分析解答.
解答 解:Ⅰ、氢氧化钙和盐酸反应生成了氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
Ⅱ、【猜想】反应可能是恰好反应,只有氯化钙(猜想二)、也可能是一种物质完全反应,另一种物质有剩余,若氢氧化钙过量,则含有氢氧化钙和氯化钙(猜想一);若盐酸过量,则含有盐酸和氯化钙(猜想三);
【进行实验】因为酚酞遇碱会变红色,而结论是猜想一不正确,即不含有氢氧化钙,故观察到的现象是溶液无明显变化(或溶液不变红色);
根据结论猜想二不正确,猜想三正确,即含有盐酸和氯化钙,其中的氯化钙溶液可以和碳酸钠溶液反应生成沉淀,稀盐酸和碳酸钠反应生成二氧化碳气体,因为碳酸钙在盐酸存在的情况下不能以沉淀的形式析出,故碳酸钠先和盐酸反应产生气泡,再和氯化钙反应产生沉淀;
【反思与拓展】(1)因为可能是完全反应,也可能是一种反应物过量,所以在分析化学反应后所得物质成分时,除考虑生成物外还需考虑:反应物的用量;
(2)因为烧杯内溶液中的溶质含有HCl显酸性,故用pH试纸测定pH应该小于7,能够使紫色的石蕊试液变成红色,但不能和排在氢后面的铜反应,虽然能够和硝酸银反应产生沉淀,但由于其中的氯化钙也能够和硝酸银产生相同的现象,不能选择,故选:ac;
(3)处理烧杯内溶液,使其溶质只含有CaCl2,碳酸钙和盐酸反应会生成氯化钙、水和二氧化碳,所以应向烧杯中加入过量的:碳酸钙.
故答案为:I、Ca(OH)2+2HCl=CaCl2+2H2O;
【猜想】可能是CaCl2和HCl;
【进行实验】溶液无明显变化(或溶液不变红色);先有气体产生,后产生沉淀;
【反思与拓展】(1)反应物的用量;
(2)ac;
(3)石灰石(或CaCO3).
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手;注意氯化钙中的盐酸只能用碳酸钙除去.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | Cl和Cl- | B. | Co和CO | C. | H和He | D. | 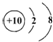 和 和  |

| A. | 门捷列夫 | B. | 拉瓦锡 | C. | 居里夫人 | D. | 诺贝尔 |
 A~H是初中化学常见的物质,其中A为白色固体,E为黑色固体(一种金属氧化物),H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.(1)写出下列物质的化学式:ACaCO3,GCuSO4,HCu(OH)2.
A~H是初中化学常见的物质,其中A为白色固体,E为黑色固体(一种金属氧化物),H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.(1)写出下列物质的化学式:ACaCO3,GCuSO4,HCu(OH)2. 小明在家自制汽水,所用的配料如图,回答下列问题.
小明在家自制汽水,所用的配料如图,回答下列问题.