题目内容
8.向H2SO4和CuSO4的混合溶液中,逐滴加入NaOH溶液,如图曲线正确的是( )| A. |  | B. |  | C. | 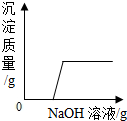 | D. | 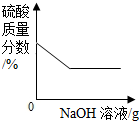 |
分析 A、根据向H2SO4和CuSO4的混合溶液中,不断加入NaOH溶液,NaOH溶液显碱性,最终溶液的PH>7进行分析;
B、根据生成硫酸钠的质量进行分析;
C、根据生成硫酸钠的质量考虑;根据开始向H2SO4和CuSO4的混合溶液中,不断加入NaOH溶液,酸碱会发生反应,不会出现氢氧化铜沉淀,当硫酸反应完毕才开始生成沉淀,当硫酸铜反应完毕,即使不断加入氢氧化钠,也不会产生沉淀了进行分析
D、根据随着氢氧化钠的不断加入,溶液的质量不断增加,H2SO4的质量分数是不断减小的进行分析.
解答 解:A、NaOH溶液显碱性,向H2SO4和CuSO4的混合溶液中,不断加入NaOH溶液,最终溶液的PH>7,图象与事实不符,故A错误;
B、由于在没加入氢氧化钠之前,没有生成硫酸钠,所以应该从0点开始,图象与事实相符,故B错误;
C、向H2SO4和CuSO4的混合溶液中,不断加入NaOH溶液,酸碱会发生中和反应,不会出现氢氧化铜沉淀,当硫酸反应完毕才开始生成沉淀,当硫酸铜反应完毕,即使不断加入氢氧化钠,也不会产生沉淀了,图象与事实相符,故C正确;
D、随着氢氧化钠的不断加入,溶液的质量不断增加,H2SO4的质量分数是不断减小,图象与事实不符,故D错误.
故选C.
点评 此题是对物质间反应的考查,解题的重点是对复分解反应的发生条件及其它反应的发生条件要有明确的认识,属基础性知识考查题.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
18.中国药学家屠呦呦研制的抗疟药青蒿素,挽救了全球数百万人的生命,她因此荣获2015年诺贝尔医学奖.下面关于青蒿素(化学式是C15H22O5)的说法正确的是( )
| A. | 青蒿素属于无机化合物 | |
| B. | 一个青蒿素分子由42个原子构成 | |
| C. | 青蒿素中氢元素的质量分数最大 | |
| D. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 |
19.下列图示实验操作中,正确的是( )
| A. | 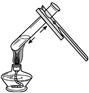 加热液体 | B. | 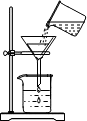 过滤 | C. | 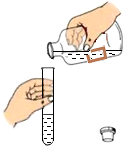 倾倒液体 | D. |  熄灭酒精灯 |
16.下列各组离子可在同一溶液中大量共存的是( )
| A. | Fe3+SO42- H+Cl- | B. | Mg2+Cl- OH- Na+ | ||
| C. | H+SO42- K+CO32- | D. | Na+Ba2+NO3 SO42- |
3.下列应用及相应原理(用化学方程式表示)都正确的是( )
| A. | 检验二氧化碳:2NaOH+CO2═Na2CO3+H2O | |
| B. | 用稀盐酸除铁锈:Fe2O3+6HCl═2FeCl3+3H2O | |
| C. | 验证铜的活动性比银强:Cu+AgNO3═CuNO3+Ag | |
| D. | 实验室用过氧化氢溶液制取氧气:2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑ |
13.图示中的“错误操作”与图下面“可能产生的后果”不一致的是( )
| A. | 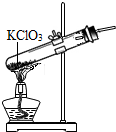 受热仪器破裂 | B. | 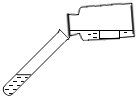 试剂外流 | C. | 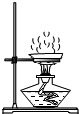 液体飞溅 | D. |  读数不正确 |
20.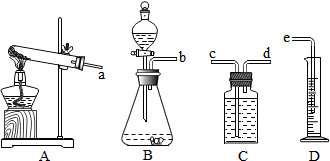 某化学学习小组,用如图所示装置制取气体.
某化学学习小组,用如图所示装置制取气体.
(1)甲同学用过氧化氢溶液和少量二氧化锰制取氧气,并通过排水量来测定所收集到氧气的体积.反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选用的实验装置接口的连接顺序为b→d→c→e.
(2)乙同学用甲的装置还可以制得另一种气体,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O(合理均可).
(3)丙同学按表中的数据,用氯酸钾加热分解制取氧气.并探究氧化铜的催化作用.用图中装置进行实验,应选的装置是ACD.为达实验目的.还需要测知的数据有气体体积、反应时间.
 某化学学习小组,用如图所示装置制取气体.
某化学学习小组,用如图所示装置制取气体.| 序号 | KC103质量 | CuO质量 |
| ① | 2.0g | 0 |
| ② | 2.0g | l.0g |
(2)乙同学用甲的装置还可以制得另一种气体,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O(合理均可).
(3)丙同学按表中的数据,用氯酸钾加热分解制取氧气.并探究氧化铜的催化作用.用图中装置进行实验,应选的装置是ACD.为达实验目的.还需要测知的数据有气体体积、反应时间.
18.下列元素中,人体摄入量过低会引起贫血的是( )
| A. | Fe | B. | Zn | C. | Na | D. | Ca |
