题目内容
6.合金是生活中广泛使用的金属材料.下列有关生活中金属的知识,不正确的是( )| A. | 优质的水龙头的内芯都使用了铜,利用了铜合金的密度大、机械加工性能好及抗腐蚀性能强的优点 | |
| B. | 不锈钢材料是在一般的钢材中加入适量的钨、锰等金属,所以抗锈蚀能力强 | |
| C. | 生铁、钢、纯铁比较,生铁的熔点最低,纯铁的硬度最低 | |
| D. | 某同学的铜制眼镜框表面出现了绿色物质(主要成分是碱式碳酸铜),可用稀盐酸除去 |
分析 合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金具有以下特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属,④合金的硬度大,熔点低.据此分析解答.
解答 解:A、多数合金没有固定的熔点,合金的熔点比组分金属低,合金与各组分金属相比一般具有更大的硬度,故A正确;
B、普通不锈钢不耐酸、碱、盐溶液等化学介质腐蚀,例:有的不锈钢放入硫酸铜溶液中,表面会生成紫红色物质,故B错误;
C、合金的熔点比各成分的熔点低,但硬度比各成分硬度高.钢是铁和碳的合金、钢的熔点比纯铁低,合金的硬度一般比成分金属大,即生铁的硬度比纯铁高.钢中碳的含量低,生铁中碳的含量高.含碳量越大,硬度越大,故C正确;
D、碱式碳酸铜(Cu2(OH)2CO3)能和盐酸反应生成可溶性的氯化铜、水和二氧化碳,故可用稀盐酸除去铜绿,故D正确;
故选B.
点评 本题考查了合金的性质,难度不大,注意构成合金的成分不一定都是金属.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.已知Si+2NaOH+H2O=Na2SiO3+2H2↑ 2Al+2NaOH+2H2O=2NaAl2+3H2↑,硅不与盐酸反应.将含铁铝硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液充分反应,测得放出氢气的质量相同.则该合金样品中铁铝硅的质量比不可能是( )
| A. | 112:27:28 | B. | 336:27:56 | C. | 28:81:7 | D. | 56:81:112 |
11.下列反应,既不属于分解反应,又不属于化合反应的是( )
| A. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | B. | 碳酸钙$\stackrel{高温}{→}$氧化钙+二氧化碳 | ||
| C. | 氢气+氧气$\stackrel{点燃}{→}$水 | D. | 锌+硫酸→硫酸锌+氢气 |
15.下列有关分子、原子、离子的说法正确的是( )
| A. | 分子是保持物质性质的粒子 | B. | 原子得失电子后形成离子 | ||
| C. | 物质都是由分子构成的 | D. | 原子是由原子核、中子、电子构成 |
16.下列各组物质,只需用组内溶液相互混合,就能鉴别出来的是( )
| A. | Na2SO4、BaCl2、KNO3、NaCl | B. | HCl、K2CO3、Ba (NO3)2、Na2SO4 | ||
| C. | NaOH、MgCl2、Na2SO4、CuSO4 | D. | KCl、AgNO3、NaCl、FeCl3 |
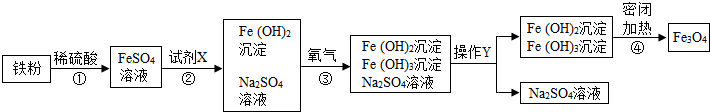 (1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是黑色.
(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是黑色.