题目内容
19.要求用化学式、化学方程式填空(1)“西气东输”中“气”的主要成分CH4
(2)我国著名化学家侯德榜发明的联合制碱法中的“碱”是Na2CO3
(3)镁条投入稀盐酸中Mg+2HCl=MgCl2+H2↑,该反应是放热 (“吸热”或”放热”)反应
(4)氯化铵与热石灰混合加热的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(5)已知浓硫酸与铜在加热条件下可发生化学反应.甲、乙两同学对该反应的生成物有不同观点.甲同学认为生成物为CuSO4和H2O,乙同学认为生成物是CuSO4、SO2和H2O,请结合信息,书写出你认为正确的反应方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O若你赞同乙同学的观点,被还原的物质是浓硫酸
(6)含氢氧化镁的药物冶疗胃酸过多的反应Mg(OH)2+2HCl═MgCl2+2H2O
(7)新鲜的蔬菜水果中主要含的营养素是水和维生素(名称)
分析 首先根据题意确定物质的化学名称,然后根据书写化学式与化学方程式的方法和步骤写出物质的化学式即可.
解答 解:(1)“西气东输”中“气”的主要成分是甲烷,故填:CH4;
(2)我国著名化学家侯德榜发明的联合制碱法中的“碱”是指纯碱,即碳酸钠;故填:Na2CO3;
(3)镁与盐酸反应生成氯化镁和氢气,此反应要放出热量,故填:Mg+2HCl=MgCl2+H2↑;放热;
(4)加热条件下,氯化铵和氢氧化钙反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.故填:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(5)浓硫酸与铜在加热条件下反应生成CuSO4、SO2和H2O,硫元素由+6变成了+4,因此浓硫酸被还原.故填:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;浓硫酸;
(6)胃液中含有盐酸,胃酸过多会引起胃部不适,可用氢氧化镁来中和过多的盐酸,化学方程式为:2HCl+Mg(OH)2═MgCl2+2H2O.
故答案为:Mg(OH)2+2HCl═MgCl2+2H2O;
(7)新鲜的蔬菜水果中主要含的营养素是水和维生素;故填:维生素.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式与化学方程式的书写是正确解答此类题的关键所在.

练习册系列答案
相关题目
7.有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其化学式为C6H8N2.下列有关对苯二胺的说法 不正确的是( )
| A. | 对苯二胺是有机化合物 | |
| B. | 对苯二胺的一个分子共有16个原子构成 | |
| C. | 对苯二胺中含有一个氮分子 | |
| D. | 对苯二胺能被皮肤少量吸收 |
14.豆浆是许多人在早餐中最喜欢的饮品,如表是豆浆中一些成分的平均质量分数:
(1)豆浆中包含了大部分得营养素,不含有的营养素只有无机盐.老年人喝豆浆可以补充钙元素,防止引起骨质疏松.
(2)成年人每天饮用250ml的豆浆(密度以1g/ml计算).则摄入钙的质量为2.5g.
| 成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素 |
| 质量分数 | 96.0 | 1.8 | 0.7 | 1.1 | 1.01 | 0.03 | 0.005 | 0.015 |
(2)成年人每天饮用250ml的豆浆(密度以1g/ml计算).则摄入钙的质量为2.5g.
3.对于Na与Na+的说法,正确的是( )
| A. | 属于同一种元素 | B. | 属于同一种粒子 | ||
| C. | 具有相同的电子层数 | D. | 核外电子数相同 |
4.某密闭容器中含有由CO和O2组成的混合气体,其中含有3N个CO和3N个O2分子,点燃充分反应后,容器中碳原子数和氧原子数之比是( )
| A. | $\frac{1}{3}$ | B. | $\frac{1}{6}$ | C. | $\frac{1}{9}$ | D. | $\frac{1}{1}$ |
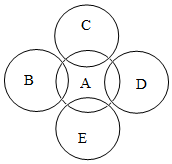 实验室有A、B、C、D、E分别是碳、硫、磷、铁、氧气五种物质中的一种,用两圆相交表示两种物质可以发生反应,其中B的固体为淡黄色,C在A中燃烧,生成的气体会使澄清的石灰水变白色浑浊,A和E反应时会冒出大量的白烟,如图,回答下列问题:
实验室有A、B、C、D、E分别是碳、硫、磷、铁、氧气五种物质中的一种,用两圆相交表示两种物质可以发生反应,其中B的固体为淡黄色,C在A中燃烧,生成的气体会使澄清的石灰水变白色浑浊,A和E反应时会冒出大量的白烟,如图,回答下列问题: