题目内容
1.化学反应在生产生活中起着重要作用.(1)氢气燃烧是人们认识物质组成的开始,该反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,检验氢气纯度时,试管口向下(填向上或向下)移近酒精灯火焰,声音很小表示气体较纯.
(2)乙炔(C2H2)也是一种燃料,5.2g C2H2与16g氧气完全燃烧生成17.6g二氧化碳和3.6g水,化学方程式为2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
分析 (1)根据氢气可燃性、验纯的方法分析回答;
(2)乙炔完全燃烧生成了二氧化碳和水,写出反应大化学方程式,根据质量守恒定律分析计算.
解答 解:(1)氢气燃烧生成了水,是人们认识物质组成的开始,该反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,检验氢气纯度时,试管口向下移近酒精灯火焰,声音很小表示气体较纯.
(2)乙炔无安全燃烧生成了二氧化碳和水,化学方程式:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,乙炔与氧气的质量比是52:160,5.2g C2H2与16g氧气恰好反应,由质量守恒定律可知,生成的水的质量为:5.2g+16g-17.6g=3.6g
故答为:(1)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;向下. (2)3.6,2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
点评 本题主要考查了根据化学方程式的书写,难度不大,化学方程式是重要的化学用语,应加强学习.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
12. 小明用如图所示装置来测定空气中氧气的含量.对该实验认识正确的是( )
小明用如图所示装置来测定空气中氧气的含量.对该实验认识正确的是( )
 小明用如图所示装置来测定空气中氧气的含量.对该实验认识正确的是( )
小明用如图所示装置来测定空气中氧气的含量.对该实验认识正确的是( )| A. | 使用红磷的量多或少,都不会影响实验结果 | |
| B. | 红磷燃烧消耗瓶内氧气,使容器内压强下降,水面上升 | |
| C. | 红磷一燃烧完,就立刻观察,并记录水进入容器的刻度 | |
| D. | 燃烧足够的红磷可使进入容器的水占容器的五分之四 |
16.我国科学家屠呦呦发现青蒿素(青蒿素分子式为C15H22O5),获2015诺贝尔医学奖.它是一种用于治疗疟疾的药物,下列说法正确的是( )
| A. | 青蒿素分子由三种元素组成 | |
| B. | 青蒿素分子含有42个原子 | |
| C. | 青蒿素中C、H、O三种元素的质量比为90:40:11 | |
| D. | 青蒿素中碳元素质量分数为63.8% |

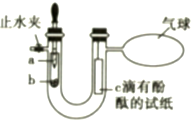 某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进:
某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进:
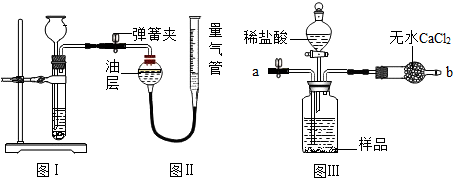
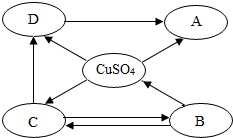 构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题: