题目内容
【题目】某化学小组对铁的冶炼、铁的锈蚀与防护进行以下实验探究. 
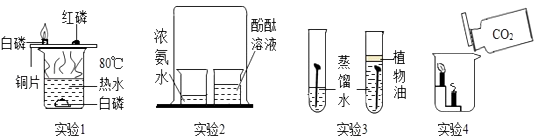
(1)该小组设计如图1研究铁的冶炼.
①试验时,应先注水片刻后再加热的目的是 .
②硬质玻璃管中发生反应的化学方程式是 .
(2)该小组有设计如图2装置,将反应所得铁粉置于锥形瓶底部,塞紧瓶塞,滴加适量食盐水,开始测量容器内压强的变化,压强与时间变化如图3所示:
①实验中食盐的作用是 .
②锥形瓶内压强下降的原因是 .
③生产、生活中铁制品的常见防锈方法有(举一例)
【答案】
(1)排净装置内的空气,以免加热时发生爆炸;Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
(2)加快了铁粉的锈蚀速率;铁锈蚀有氧气参与;在铁制品表面喷漆(合理均可)
【解析】解:(1)①实验前,装置内充满了空气,先注入水是为了先排净装置内的空气,以免加热时发生爆炸;故填:排净装置内的空气,以免加热时发生爆炸;
②氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳;故填:Fe2O3+3CO ![]() 2Fe+3CO2;(2)①食盐加快了铁粉的锈蚀速率,
2Fe+3CO2;(2)①食盐加快了铁粉的锈蚀速率,
故填:加快了铁粉的锈蚀速率;②铁的锈蚀是与空气中的水蒸气、氧气反应的过程,造成装置内压强减小,故填:铁锈蚀有氧气参与;③生活中常用的铁制品防锈方法有:在铁制品表面涂上一层保护膜,在铁制品表面镀上一层其他金属,改变铁制品的内部结构,将其制成不锈钢等合金等;故填:在铁制品表面喷漆(合理均可).
(1)根据一氧化碳还原氧化铁的注意事项以及反应原理来分析;(2)根据影响铁锈蚀的因素、装置内压强的变化以及防锈措施来分析.

练习册系列答案
相关题目