题目内容
14.用熟石灰来降低土壤的酸性,若土壤中的酸性物质以硫酸为例,写出化学方程式Ca(OH)2+H2SO4═CaSO4+2H2O.检验石灰石是否完全分解用稀盐酸和澄清的石灰水;化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2═CaCO3↓+H2O.分析 根据熟石灰(氢氧化钙的俗称)具有碱性,能用于降低土壤的酸性,氢氧化钙与硫酸反应生成硫酸钙和水;检验石灰石是否完全分解,即检验是否还含有碳酸钙,结合碳酸钙能与稀盐酸反应生成二氧化碳气体,二氧化碳气体能使澄清的石灰水变浑浊,进行分析解答.
解答 解:熟石灰(氢氧化钙的俗称)具有碱性,能用于降低土壤的酸性;氢氧化钙与硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O.
检验石灰石是否完全分解,即检验是否还含有碳酸钙,滴加稀盐酸,若产生气泡,将产生的气体通入澄清的石灰水中,澄清的石灰水变浑浊,说明还含有碳酸钙;碳酸钙能与稀盐酸反应生成二氧化碳气体,同时生成氯化钙和水,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳气体能使澄清的石灰水变浑浊,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:熟石灰;Ca(OH)2+H2SO4═CaSO4+2H2O;CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题难度不大,掌握中和反应的应用、碳酸盐的检验方法、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
4.用分子的相关知识对下列现象或事实的解释不正确的是( )
| A. | 1滴水中大约有1.67×1021个水分子,说明分子很小 | |
| B. | 水沸腾时可掀起壶盖,说明分子大小随温度升高而增大 | |
| C. | 湿衣服晾在太阳下干得快,说明分子运动速率与温度有关 | |
| D. | 600 L氧气加压后可贮存在4 L钢瓶中,说明气体分子之间间隔较大 |
5.对比是化学研究的重要方法.下列图示实验中,没有体现对比方法的是( )
| A. | 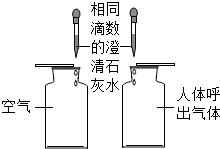 比较二氧化碳的含量 | B. | 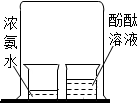 探究分子的运动 | ||
| C. | 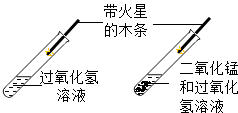 研究二氧化锰的催化作用 | D. |  区分硬水和软水 |
2.2015年我国“环境日”主题确定为“践行绿色生活”,旨在通过“环境日”的集中宣传,广泛传播和弘扬“生活方式绿色化”理念.下列做法符合“环境友好”的是( )
| A. | 为保护森林,提倡用煤做燃料 | |
| B. | 为拉动经济减少公共交通压力,提倡使用私家车出行 | |
| C. | 为提高农作物的产量,提倡大量使用化肥农药 | |
| D. | 为减少环境污染,提倡秸秆合理利用.如秸秆粉碎还田、生产沼气、作饲料、纸、作建筑装饰材料等,制定法规严禁露天焚烧秸秆 |
