题目内容
15.海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源.(1)目前世界上60%的镁是从海水中提取的.其主要步骤如下:
①提取Mg的过程中,试剂可以选用氢氧化钠.
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4.等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、过量的Na2C03溶液,过滤,再向滤液中加入适量盐酸.加入过量Na2CO3溶液的目的是除去氯化钙和过量的氯化钡.
(2)从海水中制得的氯化钠除食用外,还常用作1:业原料生产相应的化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
分析 根据还是制镁过程中加入的试剂以及粗盐提纯中各试剂的加入顺序和作用进行分析解答,根据反应物和生成物书写反应的化学返程式即可.
解答 解:(1)①提取镁的过程中,可以加入氢氧化钠与氯化镁反应,故填:氢氧化钠;
②加入过量的碳酸钠溶液能除去氯化钙,同时除去加入的过量的氯化钡,故填:除去氯化钙和过量的氯化钡;
(2)电解氯化钠的饱和溶液能生成氢氧化钠、氢气和氯气,故填:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
点评 本题考查的是海洋资源的利用,完成此题,可以依据已有的知识进行.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
5.下列各组物质中,前一种是化合物,后一种是混合物的是( )
| A. | 酒精、纯净的浓盐酸 | B. | 氢氧化钾、冰水混合物 | ||
| C. | 粗盐、澄清的石灰水 | D. | 食盐、汽油 |
3.某化学兴趣小组对某地石灰石中碳酸钙的含量进行了探究,小组成员从中取出样品10.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示.
(1)表中m=37.46;
(2)求样品中碳酸钙的质量.
| 稀盐酸的总质量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
| 烧杯中物质总质量(g) | 19.22 | 28.34 | m | 46.58 | 55.70 | 65.70 | 75.70 |
(2)求样品中碳酸钙的质量.
10.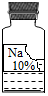 实验室有一瓶保管不当的试剂,其残缺的标签如图,这瓶试剂中的溶质不可能是:①单质②酸③碱④盐( )
实验室有一瓶保管不当的试剂,其残缺的标签如图,这瓶试剂中的溶质不可能是:①单质②酸③碱④盐( )
 实验室有一瓶保管不当的试剂,其残缺的标签如图,这瓶试剂中的溶质不可能是:①单质②酸③碱④盐( )
实验室有一瓶保管不当的试剂,其残缺的标签如图,这瓶试剂中的溶质不可能是:①单质②酸③碱④盐( )| A. | ①③ | B. | ①② | C. | ②③ | D. | ②④ |
20.利用下列各组物质之间的反应,能够验证Fe、Cu、Ag三种金属活动性顺序的是( )
| A. | Fe、CuCl2溶液、Ag | B. | FeCl2溶液、CuCl2溶液、Ag | ||
| C. | FeCl2溶液、Cu、Ag | D. | Fe、Cu、Ag、H2SO4溶液 |
4.加油站应张贴的标志是( )
| A. |  | B. |  | C. |  | D. |  |
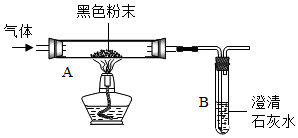 探究草酸分解的产物组成
探究草酸分解的产物组成