题目内容
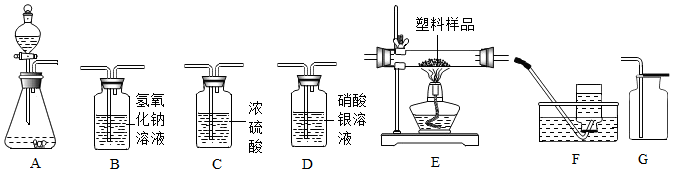
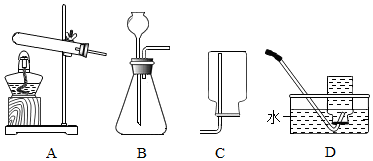
15.测定空气中氧气含量的实验中:要等装置冷却后才打开弹簧夹,原因是温度高时,气体气体膨胀,进入的水少,测定结果偏小; 如果弹簧夹未夹紧,或者塞塞子的动作 太慢,测量结果会偏大,原因部分空气受热逸出,冷却后会造成进水偏多; 不要用木炭或硫代替红磷,原因:木炭或硫燃烧生成气体,集气瓶内的压强不变.分析 用红磷燃烧测定空气的组成时,红磷一定要过量,目的是把氧气全部消耗掉;点燃红磷前,弹簧夹要夹紧胶皮管,红磷熄灭后要等集气瓶冷却后再打开弹簧夹等,由于木炭、硫燃烧生成二氧化碳、二氧化硫气体,集气瓶内压强基本不变,不能测出空气中氧气的含量.
解答 解:红磷熄灭后要等集气瓶冷却至室温再打开弹簧夹开始读数,若燃烧结束后立刻打开弹簧夹,由于剩余气体膨胀,测量的结果会小于五分之一;
如果弹簧夹未夹紧,或者塞塞子的动作太慢,会造成集气瓶内的气体受热膨胀从瓶内逸出,造成测定结果偏大;
由于木炭燃烧生成二氧化碳等气体,硫燃烧生成二氧化硫气体,造成集气瓶内压强基本不变,不能测出空气中氧气的含量.
故答案为:温度高时,气体气体膨胀,进入的水少,测定结果偏小;偏大;部分空气受热逸出,冷却后会造成进水偏多;木炭或硫燃烧生成气体,集气瓶内的压强不变.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,属于常规性实验考查题,难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
5.下列各组金属中,按金属活动性由强到弱的顺序排列正确的是( )
| A. | K Al Zn | B. | Zn Na Hg | C. | Fe Zn Al | D. | Mg Ca Cu |
10.某同学在用天平称量物体时重32.6g,称完时他发现物码放反了,但他仍然得到了准确的结果(5g 以下用游码)( )
| A. | 32.6g | B. | 31.4 g | C. | 27.4g | D. | 必须重称 |
4.小明已通过基础实验6-“粗盐的提纯”除去了难溶性杂质,查阅资料发现,实验得到的“精盐”中还含有MgCl2、Na2SO4和CaCl2可溶性杂质,他称取了一定量的“精盐”,并设计了如下实验流程再进行除杂提纯,进一步得到较纯净的NaCl固体,下列做法正确的是( )
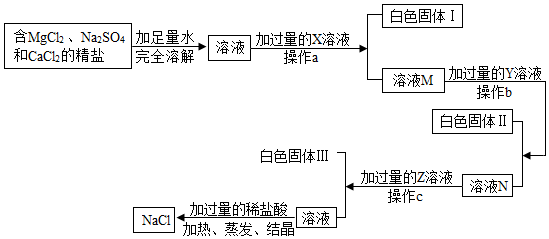

| A. | 操作a、操作b和操作c相同,都为过滤 | |
| B. | 若X、Y、Z分别为NaOH、BaCl2、Na2CO3,则溶液N中的溶质为CaCl2 | |
| C. | 若Z为Na2CO3,则白色固体一定为BaCO3和CaCO3 | |
| D. | 加入过量的稀盐酸的目的是除去过量的Na2CO3 |
5.
| 浓盐酸 | 浓硫酸 | |
| 颜色、状态、气味 | ||
| 打开瓶口现象 | ||
| 原因 |