题目内容
17.同学们做甲、乙两个中和反应实验的探究(见图).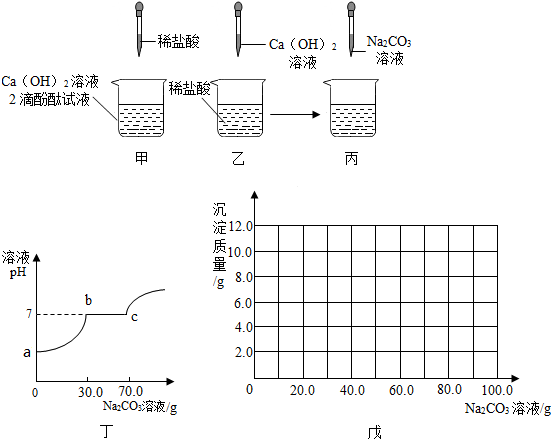
(1)取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2C03溶液(见丙图),溶液pH的变化如丁图所示.则与CaCl2反应的碳酸钠溶液的质量为40.0g;
(2)请计算该溶液中CaCl2的溶质质量分数(写出计算过程,精确到0.1%).
(3)根据计算所得数据在图戊中画出产生沉淀的曲线.
分析 稀盐酸和氢氧化钙反应生成氯化钙和水,根据提供的数据及其图象可以判断相关方面的问题.
解答 解:(1)由丁中可知,乙中稀盐酸过量,碳酸钠先和稀盐酸反应,当稀盐酸完全反应后,溶液pH=7,碳酸钠再和氯化钙反应生成碳酸钙沉淀和氯化钠,则与CaCl2反应的碳酸钠溶液的质量为:70.0g-30.0g=40.0g,
故填:40.0.
(2)设氯化钙的质量为x,生成碳酸钙的质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 111 100
40.0g×26.5% x y
$\frac{106}{40.0g×26.5%}$=$\frac{111}{x}$=$\frac{100}{y}$,
x=11.1g,y=10.0g,
该溶液中CaCl2的溶质质量分数为:$\frac{11.1g}{60.0g}$×100%=18.5%,
答:该溶液中CaCl2的溶质质量分数为18.5%.
(3)由丁中信息可知,加入30.0g碳酸钠溶液时产生沉淀,加入70.0g碳酸钠溶液时不再产生沉淀,产生沉淀的质量是10.0g,产生沉淀的曲线如下图所示: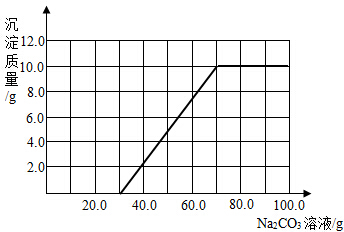
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时能够根据计算的数据准确绘图,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.下列实验现象描述不准确的是( )
| A. | 铁丝在氧气中燃烧有黑色固体生成 | |
| B. | 碳在氧气中燃烧时,伴有蓝色火焰和火星四射 | |
| C. | 物质在氧气中燃烧比在空气中燃烧更剧烈 | |
| D. | 物质在氧气中燃烧都会发光发热 |
12.景色秀丽的洪泽湖畔,矿产资源十分丰富,地产优质元明粉供不应求.元明粉的主要成分为Na2SO4,广泛用于洗涤、玻璃、造纸等行业.下表为元明粉的主要质量标准:
质检人员为确定某批产品质量等级,进行了下列实验:称取该样品28.8g(杂质为氯化钠),加100克水使其完全溶解,再向其中加入一定量的20%的BaCl2溶液恰好完全反应,过滤、洗涤、干燥,得沉淀46.6g.
(1)求反应中消耗20%的BaCl2溶液的质量.
(2)通过计算判断该批产品的质量等级最高可定为哪一级?
| 质量等级 | 特等品 | 一等品 | 二等品 | 三等品 |
| Na2SO4质量≥ | 99.3% | 99.0% | 98.0% | 95.0% |
(1)求反应中消耗20%的BaCl2溶液的质量.
(2)通过计算判断该批产品的质量等级最高可定为哪一级?
9.吸烟有害健康,其原因是香烟燃烧产生的烟气中,有一种容易与人体血红蛋白结合而使人中毒的气体,这种气体是( )
| A. | 二氧化硫 | B. | 尼古丁 | C. | 一氧化碳 | D. | 二氧化碳 |
6.下列数据为常见水果的近似pH,其中呈碱性的是( )
| A. |  菠萝pH=5.1 | B. |  杨梅pH=2.5 | C. |  苹果pH=4.1 | D. |  柿子pH=8.5 |
7.下列四个图象表示四种对应的操作过程,其中正确的是( )
| A. | 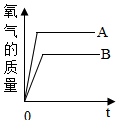 分别加热相同质量的氯酸钾和高锰酸钾制取氧气 | |
| B. | 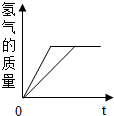 相同质量的镁,锌跟足量的稀硫酸反应制氢气 | |
| C. | 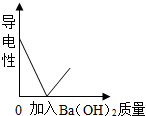 在质量一定,溶质质量分数一定的稀硫酸中逐渐加入氢氧化钡溶液 | |
| D. | 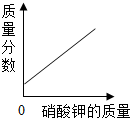 某温度下,在不饱和的稀硝酸钾溶液中,逐渐加入硝酸钾固体 |
 图A是两种元素在元素周期表中的信息,图B是氟原子的原子结构示意图.
图A是两种元素在元素周期表中的信息,图B是氟原子的原子结构示意图.

 如图所示A~F是初中化学常见的物质.图中“→”表示转化关系,“一“表示相互能反应(部分物质和反应条件未标出).其中A是紫红色金属,B常温下是气体,C是人体胃液中含有的酸.
如图所示A~F是初中化学常见的物质.图中“→”表示转化关系,“一“表示相互能反应(部分物质和反应条件未标出).其中A是紫红色金属,B常温下是气体,C是人体胃液中含有的酸.