题目内容
18.以下类推正确的是( )| A. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 氯化钠的水溶液显中性,所以所有的盐溶液都一定呈中性 | |
| C. | 点燃H2和O2混合气体可能爆炸,所以点燃CO与O2的混合气体也可能爆炸 | |
| D. | 有机物都含碳元素,所以含碳元素的化合物都是有机物 |
分析 A、酸与碱反应生成盐和水,但生成盐和水的反应不一定是中和反应;
B、根据盐溶液的性质分析;
C、根据可燃性的气体和氧气混合溶液发生爆炸分析;
D、根据有机物的定义及特殊物质分析.
解答 解:A、酸与碱生成盐和水的反应是中和反应,中和反应特指酸和碱的反应.而生成盐和水的反应不一定是中和反应.故不正确;
B、纯碱盐的水溶液显碱性,因此盐溶液不一定显中性,故错误;
C、氢气和一氧化碳都是可燃性的气体,因此和氧气混合都有可能发生爆炸,故正确;
D、有机物都含碳元素,但一氧化碳、二氧化碳等具备无机物的特征,属于无机物,故错误;
故选项为:C.
点评 酸、碱、盐是初中化学最重点的部分,在中考中占有重要地位,特别是对基本概念和理论的理解和运用,透彻理解概念是解题的必要前提.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
6.关于溶液的下列说法正确的是( )
| A. | 任何溶液都只能含有一种溶质 | |
| B. | 将硝酸钾固体溶于水时加热,既可以使硝酸钾溶得更快,又能使其溶得更多 | |
| C. | 向水中加入少量蔗糖固体可增强水的导电性 | |
| D. | 一定温度下,任何物质都可以无限制溶解在一定量的水中 |
13. 化学是在原子、分子、离子水平上研究物质及其变化的科学.
化学是在原子、分子、离子水平上研究物质及其变化的科学.
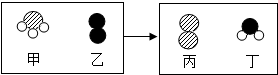
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.下列说法正确的是BE (填序号)
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
 化学是在原子、分子、离子水平上研究物质及其变化的科学.
化学是在原子、分子、离子水平上研究物质及其变化的科学.(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.下列说法正确的是BE (填序号)
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
3.下列化学用语表达错误的是( )
| A. | 亚铁离子:Fe2+ | B. | 氧原子的结构示意图: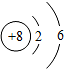 | ||
| C. | 纯碱:Na2CO3 | D. | 两个氮分子:2N |
10.下列化学用语与所表述的意义相符合的是( )
| A. | 3O-3个氧元素 | B. | $\stackrel{+3}{Fe}$-1个铁离子 | ||
| C. | O3-3个氧原子 | D. | SO3-1个三氧化硫分子 |
7.葡萄糖(C6H12O6)供给人体活动和维持体温所需能量的反应可表示为:C6H12O6+6O2$\stackrel{酶}{→}$6CO2+6H2O,下列分析错误的是( )
| A. | 葡萄糖属于高分子有机化合物 | |
| B. | 葡萄糖缓慢氧化转变成二氧化碳和水,同时产生能量 | |
| C. | 人呼出的气体和吸入的空气的成分相比,CO2和H2O的含量增加,O2的含量减少 | |
| D. | 葡萄糖氧化产生的CO2如不能及时排出人体,则血液的pH将减小 |
 “低碳生活,绿色出行”.如图为丹阳市公共自行车.请回答下列问题:
“低碳生活,绿色出行”.如图为丹阳市公共自行车.请回答下列问题: