题目内容
3.(1)某学生在探究活动中,把少量的生铁放入烧杯中并注入一定量的稀硫酸中,能观察到的现象有:生铁表面有气泡产生,溶液逐渐变浅绿色,完全反应后烧杯底部有残渣出现.请写出有关化学方程式Fe+H2SO4=FeSO4+H2↑.(2)A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,其中只有D、F为单质,它们的转化关系如下图所示(部分生成物已省略):
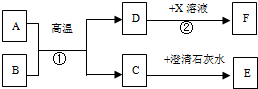
(1)写出几种物质的化学式BFe2O3,CCO2,FCu.
(2)写出反应①的方程式3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2.
分析 (1)根据生铁的组成、铁的性质、亚铁离子的颜色等方面进行分析、考虑,从而得出正确的结论.生铁是铁和碳的混合物,铁可以与酸反应,碳与酸不反应.铁与酸反应产生H2时,生成+2价的亚铁离子,而亚铁离子为浅绿色;
(2)根据A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,其中只有D、F为单质,所以F是铜,B是氧化铁,气体C会与氢氧化钙反应,所以C是二氧化碳,E是碳酸钙,所以A是碳,然后将推出的物质进行验证即可.
解答 解:(1)铁的活动性在H前面,可以与酸反应产生H2,所以生铁表面有气泡,铁在置换反应中只能生成亚铁离子,亚铁离子的颜色为浅绿色,生铁中的碳不与酸反应,因此反应后会变成残渣留在烧杯底部,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(2)A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,其中只有D、F为单质,所以F是铜,B是氧化铁,气体C会与氢氧化钙反应,所以C是二氧化碳,E是碳酸钙,所以A是碳,经过验证,推导正确,所以B是Fe2O3,C是CO2,F是Cu;
反应①是碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2.
故答案为:(1)气泡,浅绿色,残渣,Fe+H2SO4=FeSO4+H2↑;
(2)Fe2O3,CO2,Cu;
3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2.
点评 本题主要考查了生铁的组成、亚铁离子的颜色,了解常见的红色物质和C能与澄清石灰水反应,即寻找解题的突破口,然后顺藤摸瓜,进而完成其它未知物的推断.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目
14.下列关于元素的叙述中,正确的是( )
| A. | 同种原子的统称叫元素 | |
| B. | 同种元素的原子结构和质量完全相同 | |
| C. | 元素的种类取决于该元素原子的核外电子数 | |
| D. | 不同种元素的根本区别是核内质子数不同 |
18.下面的情况下一定会发生化学变化的是( )
| A. | 产生气体 | B. | 氢气和氧气混合 | ||
| C. | 发光放热 | D. | 分子破坏原子重新组合 |
12.用灯帽熄灭酒精灯,该灭火方法的主要原理是( )
| A. | 清除可燃物 | B. | 降低可燃物着火点 | ||
| C. | 隔绝空气 | D. | 使可燃物温度降到着火点以下 |
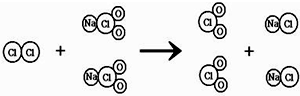 ClO2是新一代饮用水的消毒剂,我国最近成功研制出制
ClO2是新一代饮用水的消毒剂,我国最近成功研制出制