题目内容
18.图1是初中化学常见的制取气体的装置.
(1)图1中标号①的仪器名称是长颈漏斗;
(2)用高锰酸钾制取并收集氧气,应选用的装置组合是(选填字母)AC或AD,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)选择发生装置B和收集装置(选填字母)C可用于实验室制取C02,若将发生装置由B改为F,其优点是可以控制反应随时开始、随时停止;
(4)草酸受热分解生成CO、CO2和H20,实验室常用图2所示装置将其生成的C0和CO2分离并干燥.先关闭b,再打开a,则乙中排出的气体是CO;若还想获得另一种气体,应进行的操作是先关闭a,再打开b.
分析 (1)据常用仪器的名称解答;
(2)据高锰酸钾制取氧气的实验及原理解答;
(3)据实验室制取二氧化碳的实验及F装置的特点解答;
(4)CO与氢氧化钠溶液不反应,CO2氢氧化钠可反应生成碳酸钠,碳酸钠和盐酸反应可生成二氧化碳,浓硫酸具有吸水性,可干燥气体,且气体从溶液中出来时要带来部分水蒸气,故乙瓶中盛放的是浓硫酸,据此分析实验步骤
解答 解:(1)图1中标号①的仪器名称是长颈漏斗;
(2)用高锰酸钾制取并收集氧气,为固体加热反应,发生装置选择A,氧气的密度比空气大,不易溶于水,可用向上排空气法或排水法收集;反应的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取发生装置选B,二氧化碳的密度比空气大,能溶于水,收集装置选择C;若将发生装置由B改为F,其优点是可以控制反应随时开始、随时停止;
(4)要将CO和CO2分离,可在甲中装有NaOH溶液,用来吸收CO2,先分离出被乙中浓硫酸干燥过的纯净的CO,所以关闭b,打开a,混合气体进入甲装置,CO与氢氧化钠溶液不反应,可分离出 被乙中浓硫酸干燥过的纯净的CO;
二氧化碳与氢氧化钠溶液在甲中反应生成碳酸钠,要得到CO2,可在丙中盛放稀盐酸,然后关闭活塞a,打开b,从分液漏斗处加入稀盐酸,稀盐酸与碳酸钠可反应生成氯化钠、水和二氧化碳,又可分离出被乙中浓硫酸干燥过的纯净的CO2;
故答案为:(1)长颈漏斗;
(2)AC(或AD)、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)C、可以控制反应随时开始、随时停止;
(4)CO、关闭a,打开b.
点评 此题考查了氧气、二氧化碳的实验室制取方法,设计实验分离CO与CO2,掌握气体的性质是解答的关键,可先利用气体的性质加入试剂除掉一种物质,而后再把吸收后的物质与其他物质反应制取出开始除掉的气体.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )
全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )| A. | 汞的化学式为Hg | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞为非金属元素 |
| A. | 可燃性 | B. | 还原性 | C. | 氧化性 | D. | 腐蚀性 |
| A. | 生活常识 | B. | 节约意识 | ||
| C. | 安全常识 | D. | 环保意识 |
 2015年8月为了纪念抗日战争暨世界反法西斯战争胜利70周年,中国人民银行发行纪念币一套,其中面值100元的纪念币中含有0.25盎司的金.从微观角度分析,构成金的微粒是( )
2015年8月为了纪念抗日战争暨世界反法西斯战争胜利70周年,中国人民银行发行纪念币一套,其中面值100元的纪念币中含有0.25盎司的金.从微观角度分析,构成金的微粒是( )| A. | 原子 | B. | 分子 | C. | 离子 | D. | 质子 |
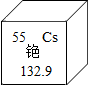
| A. | 铯原子的中子数是55 | B. | 铯原子的质子数是55 | ||
| C. | 铯元素符号为Cs | D. | 铯原子的相对原子质量为132.9 |
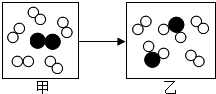 如图是某个化学反应的微观模拟图,甲表示反应前的状态,乙表示反应后的状态,下列关于该反应的说法正确的是( )
如图是某个化学反应的微观模拟图,甲表示反应前的状态,乙表示反应后的状态,下列关于该反应的说法正确的是( )| A. | 甲、乙分子总数不变 | B. | 乙比甲原子总数减少 | ||
| C. | 甲的质量大于乙的质量 | D. | 该反应是化合反应 |
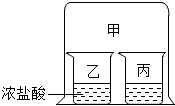 如图所示.小烧杯乙中盛有浓盐酸.在小烧杯丙中加入某种溶液后,立即用大烧杯甲罩住小烧杯乙和丙,烧杯丙中出现了明显变化.则烧杯丙中加入的溶液可能是B
如图所示.小烧杯乙中盛有浓盐酸.在小烧杯丙中加入某种溶液后,立即用大烧杯甲罩住小烧杯乙和丙,烧杯丙中出现了明显变化.则烧杯丙中加入的溶液可能是B