题目内容
9.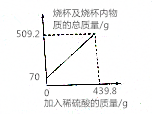 为测定某含铁样品中铁的质量分数,现取一定质量的样品粉末于质量为50g的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入439.8g稀硫酸时反应恰好完全(样品中杂质不与稀硫酸反应),加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图所示,计算:
为测定某含铁样品中铁的质量分数,现取一定质量的样品粉末于质量为50g的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入439.8g稀硫酸时反应恰好完全(样品中杂质不与稀硫酸反应),加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图所示,计算:(1)该实验取用的样品质量为20g.
(2)样品中铁的质量分数.
(3)反应结束以后滤液中溶质的质量分数.(计算结果精确到小数点后一位)
分析 铁与稀硫酸反应生成硫酸亚铁溶液和氢气,由加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,根据质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,据此根据反应的化学方程式列式计算出参加反应铁的质量、生成硫酸亚铁的质量,进而计算出样品中铁的质量分数、反应结束以后滤液中溶质的质量分数.
解答 解:(1)该实验取用的样品质量为70g-50g=20g.
(2)由质量守恒定律,生成氢气的质量为70g+439.8g-509.2g=0.6g.
设参加反应铁的质量为x,生成硫酸亚铁的质量为y,
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.6g
$\frac{56}{2}=\frac{x}{0.6g}$ x=16.8g
样品中铁的质量分数为$\frac{16.8g}{20g}$×100%=84%.
(3)$\frac{152}{2}=\frac{y}{0.6g}$ y=45.6g
反应结束以后滤液中溶质的质量分数为$\frac{45.6g}{16.8g+439.8g-0.6g}$×100%=10%.
答:(1)20;(2)样品中铁的质量分数为84%;(3)反应结束以后滤液中溶质的质量分数为10%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
19.氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B 中,并进行了如下图所示的三组实验.

(1)实验l 中,两支试管的溶液都变成红色.
(2)实验2中,两支试管中的现象均为为生成蓝色沉淀.
(3)实验3中,李红同学向两支试管吹气,A 中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.B 中无现象,为了探究吹气后B 中溶质的成分,李红进行了如下探究.
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠…
实验和结论:
反思与评价:
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必须要换试剂,将氢氧化钙 溶液换成氯化钙溶液.

(1)实验l 中,两支试管的溶液都变成红色.
(2)实验2中,两支试管中的现象均为为生成蓝色沉淀.
(3)实验3中,李红同学向两支试管吹气,A 中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.B 中无现象,为了探究吹气后B 中溶质的成分,李红进行了如下探究.
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠…
实验和结论:
| 实验 | 实验现象 | 结论 |
| 取B 中少量溶液,加入澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液. | 产生白色沉淀,溶液呈现红色. | 猜想3成立 |
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必须要换试剂,将氢氧化钙 溶液换成氯化钙溶液.
20.应用储能介质(某种结晶水合物)储存和再利用太阳能是一项新技术,其原理是:当白天阳光照射时,储能介质熔化,同时吸收热能.当夜晚环境温度降低时,储能介质凝固,同时释放出热能,某地区的白天气气温可达40℃,夜晚可下降至-10℃以下,根据上述原理和表中几种常见储能介质的有关数据,该地区应用上述技术调节室温时,选用储能介质最好是( )
| 结晶水合物 | 熔点/℃ | 熔化时吸热/(KJ•g-1) | |
| A | CaCl2•6H2O | 29.0 | 0.172 |
| B | Na2SO4•10H2O | 32.4 | 0.269 |
| C | Na2HPO4•12H2O | 36.1 | 0.282 |
| D | Na2S2O3•5H2O | 48.5 | 0.200 |
| A. | A | B. | B | C. | C | D. | D |
4.某些花岗岩石中含有放射性元素氡.一种氡原子的质子数为86,相对原子质量为222,这种原子核外电子数和中子数分别为( )
| A. | 50,86 | B. | 86,50 | C. | 136,50 | D. | 86,136 |