题目内容
实验室通常用如图所示的两套装置,用不同的方法来制氧气.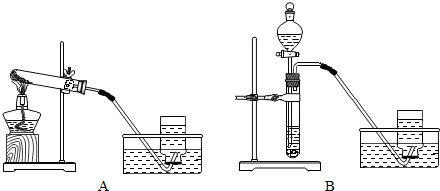
(1)A、B装置中收集气体的方法叫做 .
(2)若采用装置B制取氧气,在分液漏斗中应盛放的液体药品是 ,反应的化学方程式为 ,B装置中采用分液漏斗的优点是(只要求写出一点): .
(3)若采用装置A制取氧气,反应的化学方程式为 ,给大试管加热时要先 ,然后 .停止加热时,先要 ,然后 .
(4)检验氧气的方法是 .

(1)A、B装置中收集气体的方法叫做
(2)若采用装置B制取氧气,在分液漏斗中应盛放的液体药品是
(3)若采用装置A制取氧气,反应的化学方程式为
(4)检验氧气的方法是
考点:氧气的制取装置,氧气的收集方法,氧气的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)收集气体的方法包括:排水法和排空气法;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
利用加热的方法制取氧气,并且利用排水法收集氧气时,要按照一定的步骤进行,特别是要注意集满氧气后的操作顺序,以防发生安全事故;
(4)氧气能够支持燃烧,能使带火星的木条复燃.
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
利用加热的方法制取氧气,并且利用排水法收集氧气时,要按照一定的步骤进行,特别是要注意集满氧气后的操作顺序,以防发生安全事故;
(4)氧气能够支持燃烧,能使带火星的木条复燃.
解答:解:(1)A、B装置中收集气体的方法叫排水法.
故填:排水法.
(2)若采用装置B制取氧气,应该利用过氧化氢分解制取,过氧化氢在二氧化锰的催化作用下分解的化学方程式为:2H2O2
2H2O+O2↑,B装置中采用分液漏斗的优点是能够控制反应速率,节约液体药品.
故填:过氧化氢溶液;2H2O2
2H2O+O2↑;能够控制反应速率.
(3)若采用装置A制取氧气,应该利用高锰酸钾受热分解制取,高锰酸钾受热分解的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;
给大试管加热时要先预热,然后对准药品部位加热,这样可以防止试管炸裂;
停止加热时,先要把导气管移出水面,然后熄灭酒精灯,这样可以防止炸裂试管.
故填:2KMnO4
K2MnO4+MnO2+O2↑;预热;对准药品部位加热;把导气管移出水面,熄灭酒精灯.
(4)检验氧气的方法是:把带火星的木条伸入集气瓶中,带火星的木条复燃.
故填:把带火星的木条伸入集气瓶中,带火星的木条复燃.
故填:排水法.
(2)若采用装置B制取氧气,应该利用过氧化氢分解制取,过氧化氢在二氧化锰的催化作用下分解的化学方程式为:2H2O2
| ||
故填:过氧化氢溶液;2H2O2
| ||
(3)若采用装置A制取氧气,应该利用高锰酸钾受热分解制取,高锰酸钾受热分解的化学方程式为:2KMnO4
| ||
给大试管加热时要先预热,然后对准药品部位加热,这样可以防止试管炸裂;
停止加热时,先要把导气管移出水面,然后熄灭酒精灯,这样可以防止炸裂试管.
故填:2KMnO4
| ||
(4)检验氧气的方法是:把带火星的木条伸入集气瓶中,带火星的木条复燃.
故填:把带火星的木条伸入集气瓶中,带火星的木条复燃.
点评:本题综合考查了学生的基本实验能力,涉及收集气体的方法、化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答.

练习册系列答案
相关题目
用分子、原子的观点分析下列生活中的现象,其解释不合理的是( )
| A、水结成冰---分子停止运动 |
| B、八月桂花飘香---分子在不断运动 |
| C、1滴水中约含1.67×1021个水分子---分子很小 |
| D、50mL水与50mL酒精混合后,总体积小于100mL---分子之间有间隔 |
对于化学反应xA+yB═mC+nD,下列说法正确的是( )
| A、化学计量数x与y之和一定等于m与n的和 |
| B、若反应物A、B各为a g,生成物C和D总质量不一定是2a g |
| C、反应物A与B的质量比,一定等于生成物C和D的质量比 |
| D、若生成物C是单质,D是化合物,则A、B中必定也是一个单质,一个化合物 |
如图所示,分别表示4个实验过程中某些质量的变化,其中正确的是( )
A、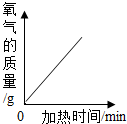 加热一定质量的高锰酸钾固体 |
B、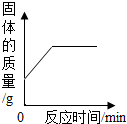 铜丝在空气中加热 |
C、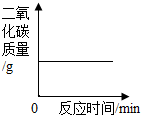 木炭在盛有氧气的密闭容器内燃烧 |
D、 电解水生成两种气体 |