题目内容
8.某碳酸钠样品中混有少量氯化钠,根据如图所示信息计算该样品中碳酸钠的质量分数.(计算结果精确到0.1%)(反应的化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl)
分析 根据氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,然后结合题中所给的数据进行计算.
解答 解:设该样品中碳酸钠的质量为x,
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{x}$=$\frac{100}{5g}$
x=5.3g
样品中碳酸钠的质量分数为:$\frac{5.3g}{7.5g}$×100%=70.7%.
答:设该样品中碳酸钠的质量为70.7%.
点评 本题难度不大,考查同学们灵活运用化学方程式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
18.下列化学方程式和对应的反应类型均正确的是( )
| A. | 4P+O2=2P2O5 化合反应 | |
| B. | H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ 分解反应 | |
| C. | C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2 置换反应 | |
| D. | HCl+NaOH=NaCl+H2O 复分解反应 |
16.下列化学用语与含义不相符的是( )
| A. | 02---氧离子 | B. | 3H--3个氢元素 | ||
| C. | Fe304--四氧化三铁 | D. | 2N2--2个氮气分子 |
3.下列鉴别物质所用的方法或试剂,错误的是( )
| A. | 氧气和氮气-观察颜色 | B. | 铁粉和炭粉-用稀硫酸 | ||
| C. | 羊毛和化学纤维-点燃闻气味 | D. | 氢氧化钠溶液和水-用酚酞溶液 |
13.从分子的角度分析并解释下列事实,不正确的是( )
| 选项 | 事实 | 解释 |
| A | 碘酒是混合物 | 由不同种分子构成 |
| B | 端午时节粽飘香 | 分子在不断运动着 |
| C | 气体受热膨胀 | 温度升高,分子自身体积增大 |
| D | 固体碘受热升华 | 碘分子间的间隔变大 |
| A. | A | B. | B | C. | C | D. | D |
17.某同学用pH试纸测得以下液体的pH,实验过程中pH试纸变成蓝色的是( )
| A. | 雨水pH=6 | B. | 食醋pH=3 | C. | 肥皂水pH=10 | D. | 食盐水pH=7 |
 A、B、C是中学化学常见的化合物,A、B、C的转化关系如图所示,请回答下列问题:
A、B、C是中学化学常见的化合物,A、B、C的转化关系如图所示,请回答下列问题:
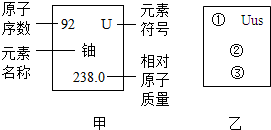 科学家发现一种新元素,该元素原子核外电子数为117,中子数为174,相对原子质量为291,元素名称Ununseptium,符号Uus,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
科学家发现一种新元素,该元素原子核外电子数为117,中子数为174,相对原子质量为291,元素名称Ununseptium,符号Uus,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )