题目内容
15.如图是一些物质间的转换关系(提示:二氧化锰不溶于水),请回答下列问题: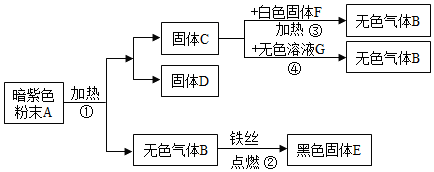
(1)写出下列物质的名称:B氧气,F氯酸钾,G过氧化氢
(2)写出反应④的表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,实验②中预先加水的目的是防止生成物熔化溅落下来使瓶底炸裂
(3)固体C在反应③、④中起到催化作用.
分析 暗紫色粉末A加热分解生成固体C和D、无色气体B,铁丝在B中能燃烧生成黑色固体E,结合铁在氧气中燃烧生成四氧化三铁,则B为氧气;高锰酸钾是暗紫色粉末,在加热条件下生成锰酸钾、二氧化锰和氧气,则A为高锰酸钾;C与白色固体F加热生成氧气,与无色液体G混合产生氧气,结合氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,过氧化氢在二氧化锰的催化作用下生成水和氧气,则C为二氧化锰,D为锰酸钾,F为氯酸钾、G为过氧化氢;据此进行分析解答.
解答 解:暗紫色粉末A加热分解生成固体C和D、无色气体B,铁丝在B中能燃烧生成黑色固体E,由铁在氧气中燃烧生成四氧化三铁,则B为氧气;高锰酸钾是暗紫色粉末,在加热条件下生成锰酸钾、二氧化锰和氧气,则A为高锰酸钾;C与白色固体F加热生成氧气,与无色液体G混合产生氧气,由氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,过氧化氢在二氧化锰的催化作用下生成水和氧气,则C为二氧化锰,D为锰酸钾,F为氯酸钾、G为过氧化氢.
(1)BFG的名称是氧气、氯酸钾、过氧化氢.
(2)反应④,即过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
实验②中预先加水的目的是防止生成物熔化溅落下来使瓶底炸裂.
(3)固体C(二氧化锰)在反应③、④中起到催化作用.
故答案为:(1)氧气、氯酸钾、过氧化氢;(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;防止生成物熔化溅落下来使瓶底炸裂;(3)催化.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

| A. | 密度小于空气,难溶于水 | B. | 密度大于空气,难溶于水 | ||
| C. | 密度小于空气,易溶于水 | D. | 密度大于空气,极易溶于水 |
| A. | 硫在氧气中燃烧 | B. | 石蜡在空气中燃烧 | ||
| C. | 木炭在氧气中燃烧 | D. | 铁丝在氧气中燃烧 |
| A. | 30mL | B. | 大于30mL | C. | 小于30mL | D. | 无法确定 |
| A. | 氧气能和许多物质反应,所以氧气是化学性质比较活泼的气体 | |
| B. | 铁在氧气中燃烧生成氧化铁 | |
| C. | 给氯酸钾加热,若不加二氧化锰就不产生氧气 | |
| D. | 课本上测定空气中氧气含量的实验中,若将红磷换成木炭实验会失败 |
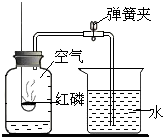 “空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开弹簧夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开弹簧夹,水注入集气瓶.回答下列问题: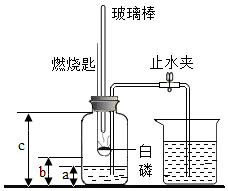 某化学研究性学习小组在学习了“空气中氧气含量测定”实验后,他们查阅资料发现磷燃烧生成的白烟(五氧化二磷)对人体有害,于是他们再课本实验的基础上改进了教材中的实验,设计出如图所示的实验装置.实验步骤如下:
某化学研究性学习小组在学习了“空气中氧气含量测定”实验后,他们查阅资料发现磷燃烧生成的白烟(五氧化二磷)对人体有害,于是他们再课本实验的基础上改进了教材中的实验,设计出如图所示的实验装置.实验步骤如下: