题目内容
有A、B、C、D、E五种元素,A的单质是空气中含量最多的气体:B、C分别是地壳中含量最多的非金属元素和金属元素;D在空气中燃烧产生大量白烟,在军事上可作烟幕弹;E元素的单质可在B元素形成的单质中燃烧,产生蓝紫色火焰.
(1)用元素符号表示:A
(2)由B、C、E三种元素形成的化合物的化学式是
(1)用元素符号表示:A
N
N
,BO
O
,CAl
Al
,DP
P
.(2)由B、C、E三种元素形成的化合物的化学式是
Al2(SO4)3
Al2(SO4)3
.分析:根据空气中各成分的体积分数考虑空气中含量最多的气体;根据地壳中最多的前五种元素考虑地壳中含量最多的非金属元素和金属元素;根据磷在空气中燃烧的现象、硫在氧气中燃烧的现象考虑本题.
解答:解:(1)空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%,所以空气中最多的气体是氮气,所以A是N元素;地壳中最多的前五种元素是:O、Si、Al、Fe、Ca,所以地壳中含量最多的非金属元素是O,地壳中含量最多的金属元素是Al;磷在空气中燃烧生成大量白烟,因为磷燃烧的生成物是五氧化二磷,属于白色固体,白烟就是白色固体颗粒,所以D是P元素,硫在氧气中燃烧,发出蓝紫色火焰,放出热量,生成有刺激性气味的气体,所以E是S元素;
(2)B、C、E分别是O、Al、S;O和S能形成硫酸根,化合价为-2价,Al为+3价,正价在前,负价在后,十字交叉再约简,所以化学式为Al2(SO4)3
故答案为:(1)N;O;Al;P;(2)Al2(SO4)3.
(2)B、C、E分别是O、Al、S;O和S能形成硫酸根,化合价为-2价,Al为+3价,正价在前,负价在后,十字交叉再约简,所以化学式为Al2(SO4)3
故答案为:(1)N;O;Al;P;(2)Al2(SO4)3.
点评:解答本题关键是要知道空气中各成分即体积分数,了解地壳中前几种元素,知道磷、硫燃烧时的现象,熟悉化学式的写法,尤其是带有原子团的化学式的写法,原子团个数不为1必须加括号.

练习册系列答案
相关题目

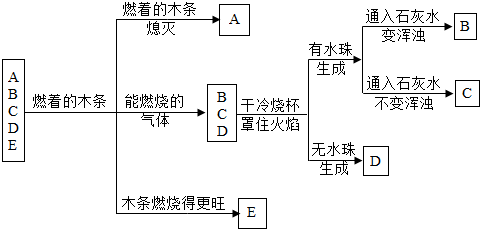

 有A、B、C、D、E五种常见物质,它们有如图所示的关系:已知:C是一种金属,气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结合,推断B物质的化学式:
有A、B、C、D、E五种常见物质,它们有如图所示的关系:已知:C是一种金属,气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结合,推断B物质的化学式: