题目内容
8.为了测定某蛋壳中碳酸钙的质量分数,小强同学进行了如下实验:称取10g洁净干燥的蛋壳碎屑放在烧杯里,然后加人足量的稀盐酸90g,充分反应后,称得烧杯中反应剩余物为97.14g.(假设其他物质不与盐酸反应,气体全部逸出)(1)反应中生成二氧化碳的质量是多少?(2)10g蛋壳中碳酸钙的质量分数是多少?
(3)应后烧杯中所得溶液的溶质质量分数是多少?
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳质量,据此根据反应的化学方程式列式计算出参加反应碳酸钙的质量、生成氯化钙的质量,进而计算出碳酸钙的质量分数、所得溶液的溶质质量分数.
解答 解:(1)由质量守恒定律,反应中生成二氧化碳的质量是10g+90g-97.14g=2.86g.
(2)设参加反应碳酸钙的质量为x,生成氯化钙的质量为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 2.86g
$\frac{100}{44}=\frac{x}{2.86g}$ x=6.5g.
10g蛋壳中碳酸钙的质量分数是$\frac{6.5g}{10g}×$100%=65%.
(3)$\frac{111}{44}=\frac{y}{2.86g}$ y=7.125g
应后烧杯中所得溶液的溶质质量分数是$\frac{7.125g}{6.5g+90g-2.86g}$×100%≈7.6%.
答:(1)反应中生成二氧化碳的质量是2.86g;(2)10g蛋壳中碳酸钙的质量分数是65%;(3)应后烧杯中所得溶液的溶质质量分数是7.6%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
19.如图所示有关粒子结构示意图的说法不正确的是( )
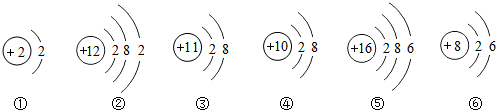

| A. | ①和②化学性质相似 | B. | ②和⑤属于同一周期的原子 | ||
| C. | ①③④具有相对稳定结构 | D. | ①④⑤⑥属于非金属元素的原子 |
4.酸、碱在生活、生产中有着重要的用途,请按要求填表.
| 物质类别 | 物质名称 | 化学式 | 用途 |
| 酸 | 氯化氢 | HCl | 除铁锈 |
| 碱 | 火碱 | NaOH | 除油污 |
| 碱 | 氢氧化钙 | Ca(OH)2 | 改良酸性土壤 |
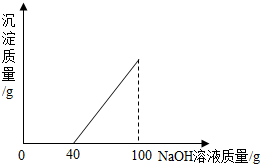 在硫酸与硫酸铜的混合溶液200克中,滴入40%的氢氧化钠溶液100克,恰好完全反应.记录反应过程,得到的沉淀与所加的氢氧化钠溶液的质量关系如图所示.
在硫酸与硫酸铜的混合溶液200克中,滴入40%的氢氧化钠溶液100克,恰好完全反应.记录反应过程,得到的沉淀与所加的氢氧化钠溶液的质量关系如图所示.