题目内容
有人用经过粉碎的含较多有机物杂质的粗铜,通过如图1步骤制取硫酸铜晶体.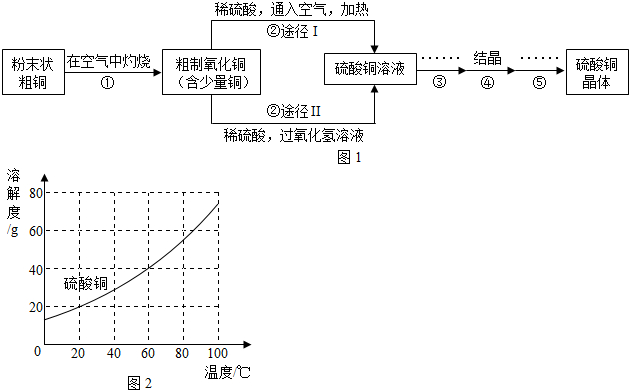
(1)若步骤①灼烧温度过高会产生副产物氧化亚铜(铜为+1价),其化学式为 ;
(2)写出步骤②中氧化铜与稀硫酸反应的化学方程式: ;
(3)步骤②中,铜与稀硫酸不能直接发生置换反应的原因是 ;
(4)反应途径Ⅰ和Ⅱ,分别有下列反应发生:
途径Ⅰ:2Cu+O2+2H2SO4
2CuSO4+2H2O
途径Ⅱ:Cu+H2O2+H2SO4═CuSO4+2H2O
请选择你认为更合适于实际应用的途径,并说明理由: ;
(5)根据图2,步骤④的结晶方法是 ;
(6)若800kg粗制氧化铜(其中单质铜的质量分数为4%)通过途径Ⅱ转化为硫酸铜,计算参加反应的过氧化氢的质量.(写出计算过程)

(1)若步骤①灼烧温度过高会产生副产物氧化亚铜(铜为+1价),其化学式为
(2)写出步骤②中氧化铜与稀硫酸反应的化学方程式:
(3)步骤②中,铜与稀硫酸不能直接发生置换反应的原因是
(4)反应途径Ⅰ和Ⅱ,分别有下列反应发生:
途径Ⅰ:2Cu+O2+2H2SO4
| ||
途径Ⅱ:Cu+H2O2+H2SO4═CuSO4+2H2O
请选择你认为更合适于实际应用的途径,并说明理由:
(5)根据图2,步骤④的结晶方法是
(6)若800kg粗制氧化铜(其中单质铜的质量分数为4%)通过途径Ⅱ转化为硫酸铜,计算参加反应的过氧化氢的质量.(写出计算过程)
考点:物质的相互转化和制备,结晶的原理、方法及其应用,金属的化学性质,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:物质的制备
分析:(1)根据化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零解答;
(2)根据氧化铜可以和稀硫酸反应生成蓝色的硫酸铜溶液,同时生成了水,可以据此完成解答;
(3)根据金属铜在金属活动性顺序表中处于H元素后,不能跟稀硫酸发生反应解答;
(4)根据反应途径分析解答;
(5)根据硫酸铜的溶解度随温度的升高而增大解答;
(6)根据铜的质量利用化学方程求出过氧化氢的质量.
(2)根据氧化铜可以和稀硫酸反应生成蓝色的硫酸铜溶液,同时生成了水,可以据此完成解答;
(3)根据金属铜在金属活动性顺序表中处于H元素后,不能跟稀硫酸发生反应解答;
(4)根据反应途径分析解答;
(5)根据硫酸铜的溶解度随温度的升高而增大解答;
(6)根据铜的质量利用化学方程求出过氧化氢的质量.
解答:解:
(1)氧化亚铜中铜元素显+1价,氧元素显-2价,其化学式为Cu2O;
(2)氧化铜可以和稀硫酸反应生成蓝色的硫酸铜溶液,所以可以观察到黑色粉末消失,溶液呈蓝色;该反应同时生成了水,该反应的化学方程式为:H2SO4+CuO═CuSO4+H2O;
(3)根据金属活动性顺序表,金属铜在金属活动性顺序表中处于H元素后,不能跟稀硫酸发生反应;
(4)由反应途径Ⅰ和Ⅱ相比较各自有各自的优点,途径Ⅰ:原料之一为空气,生产成本较低;或途径Ⅱ:反应不需加热,操作相对简便,节约能源;
(5)硫酸铜的溶解度随温度的升高而增大,适合的结晶方法是冷却;
(6)800kg粗制氧化铜中单质铜的质量为:800kg×4%=32kg
设参加反应的过氧化氢的质量为x
Cu+H2O2+H2SO4═CuSO4+2H2O
64 34
32kg x
=
x=17kg
参加反应的过氧化氢的质量为17kg.
答案:
(1)Cu2O;
(2)H2SO4+CuO═CuSO4+H2O;
(3)金属铜在金属活动性顺序表中处于H元素后;
(4)途径Ⅰ.原料之一为空气,生产成本较低;或途径Ⅱ.反应不需加热,操作相对简便,节约能源;
(5)降温结晶;
(6)参加反应的过氧化氢的质量为17kg.
(1)氧化亚铜中铜元素显+1价,氧元素显-2价,其化学式为Cu2O;
(2)氧化铜可以和稀硫酸反应生成蓝色的硫酸铜溶液,所以可以观察到黑色粉末消失,溶液呈蓝色;该反应同时生成了水,该反应的化学方程式为:H2SO4+CuO═CuSO4+H2O;
(3)根据金属活动性顺序表,金属铜在金属活动性顺序表中处于H元素后,不能跟稀硫酸发生反应;
(4)由反应途径Ⅰ和Ⅱ相比较各自有各自的优点,途径Ⅰ:原料之一为空气,生产成本较低;或途径Ⅱ:反应不需加热,操作相对简便,节约能源;
(5)硫酸铜的溶解度随温度的升高而增大,适合的结晶方法是冷却;
(6)800kg粗制氧化铜中单质铜的质量为:800kg×4%=32kg
设参加反应的过氧化氢的质量为x
Cu+H2O2+H2SO4═CuSO4+2H2O
64 34
32kg x
| 64 |
| 32 |
| 32kg |
| x |
x=17kg
参加反应的过氧化氢的质量为17kg.
答案:
(1)Cu2O;
(2)H2SO4+CuO═CuSO4+H2O;
(3)金属铜在金属活动性顺序表中处于H元素后;
(4)途径Ⅰ.原料之一为空气,生产成本较低;或途径Ⅱ.反应不需加热,操作相对简便,节约能源;
(5)降温结晶;
(6)参加反应的过氧化氢的质量为17kg.
点评:据生产流程图,正确理解每个过程在生产中的作用,从而达到全面掌握生产过程的目的,为解答问题做足准备.

练习册系列答案
相关题目
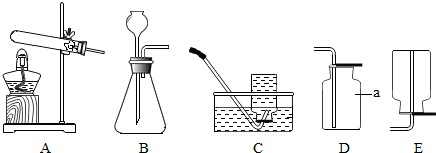
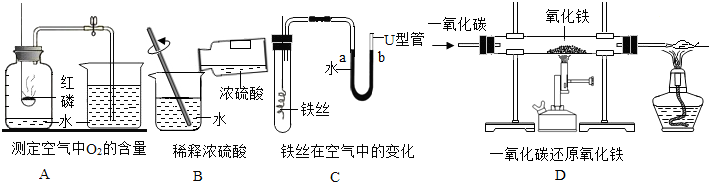
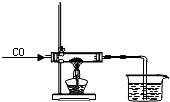 如图进行实验,如果硬质试管中的药品是CuO,实验现象为
如图进行实验,如果硬质试管中的药品是CuO,实验现象为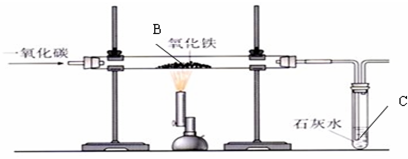
 近日,有报道称,一款名为“阿拉伯茶”的新型毒品,在去年开始已经流入中国的地下毒品交易市场.这种植物从外表上来看与苋菜非常相似,吸食者可以像吃生菜一样嚼食,但毒效却是相当的惊人.有关信息如图,请回答下列问题:
近日,有报道称,一款名为“阿拉伯茶”的新型毒品,在去年开始已经流入中国的地下毒品交易市场.这种植物从外表上来看与苋菜非常相似,吸食者可以像吃生菜一样嚼食,但毒效却是相当的惊人.有关信息如图,请回答下列问题: