题目内容
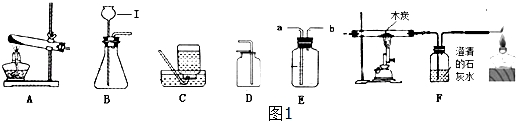
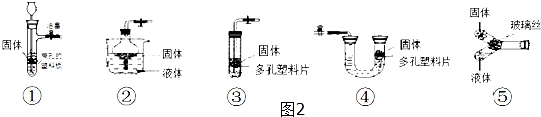
某白色固体可能是煅烧碳酸钙后的剩余物,为确定其成分,进行如下实验:
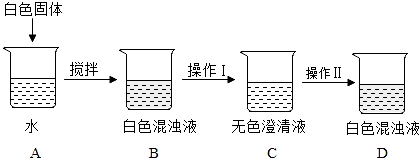
①高温煅烧碳酸钙的化学方程式是 ;
②分离B中难溶物的操作Ⅰ是 ;
③操作Ⅱ的目的是 ,D中白色固体可能是 ;
④为达到实验目的,还应进行的操作是 .
【考点】盐的化学性质;生石灰的性质与用途;书写化学方程式、文字表达式、电离方程式.
【专题】常见的盐 化学肥料.
【分析】①根据碳酸钙在高温的条件下生成氧化钙和二氧化碳进行分析;
②根据过滤可以将不溶物和可溶物分离进行分析;
③根据氧化钙和水反应会生成氢氧化钙,碳酸钙难溶于水进行分析;
④根据碳酸钙和盐酸反应会生成二氧化碳进行分析.
【解答】解:①碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3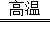 CaO+CO2↑;
CaO+CO2↑;
②过滤可以将不溶物和可溶物分离,所以分离B中难溶物的操作Ⅰ是过滤;
③氧化钙和水反应会生成氢氧化钙,碳酸钙难溶于水,所以操作Ⅱ的目的是检验原混合物中是否有氧化钙(C中是否有氢氧化钙),D中白色固体可能是碳酸钙;
④碳酸钙和盐酸反应会生成二氧化碳,所以为达到实验目的,还应进行的操作是:取煅烧后的固体(或B中过滤后的固体),加入足量稀盐酸,产生气泡则剩余固体中含有碳酸钙.
故答案为:①CaCO3 CaO+CO2↑;
CaO+CO2↑;
②过滤;
③检验原混合物中是否有氧化钙(C中是否有氢氧化钙),碳酸钙;
④取煅烧后的固体(或B中过滤后的固体),加入足量稀盐酸,产生气泡则剩余固体中含有碳酸钙.
【点评】本考点考查了物质组成成分的探究,对产物进行探究,属于实验方法和过程的探究.本题还对实验进行了评价,这类探究实验要具体问题具体分析,根据步骤中不同的现象去思考、去探究,从而回答题目给出的问题,书写化学方程式时,要注意配平.


练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目

 元素 C.原子 D.分子
元素 C.原子 D.分子