题目内容
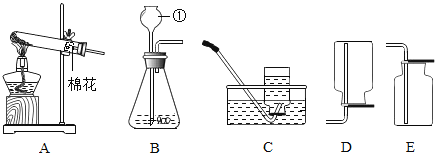
【题目】一名同学把“十一”去祖山旅游时灌装的一瓶山泉水带到实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水。
请回答下列问题:

(1)取水后加入明矾的作用是________。
(2)进行过滤操作时,下列做法错误的是 ______。
A.玻璃棒要靠在三层滤纸的一边 B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口 D.液面不要低于滤纸边缘
(3)向滤液中加入活性炭,利用其 ______性,除去水样中的色素和异味。
(4)消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为_______。
(5)在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是__________________
(6)对于静置、吸附、过滤、蒸馏等净化水的操作,①上述操作中,净化程度由高到低的顺序是 ____________;②可以降低水硬度的是______。
【答案】 利用明矾溶于水后生成的胶状物对杂质的吸附,使杂质沉降来达到净水的目的(或吸附水中的悬浮杂质,使之沉降)。 D 吸附 +6 防止加热时出现暴沸 蒸馏、吸附、过滤、静置 ② 蒸馏
【解析】(1)由于明矾溶于水的生成物具有吸附性,取水后加入明矾的作用是吸附悬浮杂质、加速沉降;(2)进行过滤操作时,玻璃棒靠在三层滤纸的一边、漏斗下端的管口要紧靠烧杯的内壁、滤纸的边缘要低于漏斗口、液面要低于滤纸边缘等,所以D错误;(3)向滤液中加入活性炭,利用其吸附性,除去水样中的色素和异味;(4)在Na2FeO4中,Na元素的化合价为+1价,O元素的化合价为2价,设该化合物中Fe元素的化合价为x,由化学式和化合物中正负化合价的代数和为0,则(+1)×2+x+(2)×4=0,解得x=+6;(5)在制取蒸馏水的过程中,在水中放碎瓷片,其作用是防止加热时出现暴沸;(6) ①在各种净水的方法中净化程度最高的是蒸馏,次之是吸附,再次之是过滤,最低的是静置;②能使硬水的硬度变软的操作是蒸馏,它可以除掉可溶性的钙、镁化合物。