题目内容
4. A、B、C三种物质的溶解度曲线如图所示,回答下列问题:
A、B、C三种物质的溶解度曲线如图所示,回答下列问题:(1)t1℃时,将30gA放入100g水中,充分搅拌后,所得溶液中溶质和溶剂的质量比为1:5;
(2)t2℃时,将26gA物质、29gB物质同时放入100g水中,降温至t1℃,能析出晶体的物质是A;
(3)大量A物质中含有少量B物质,可以用降温结晶(或冷却热饱和溶液)的方法提纯A物质.
分析 (1)据该温度下A 的溶解度分析解答;
(2)据溶液中溶质的质量和降温后AB的溶解度分析解答;
(3)据AB的溶解度受温度影响大小分析判断.
解答 解:(1)t1℃时A的溶解度是20g,即100g水中最多溶解20g的A,所以将30gA放入100g水中,充分搅拌后剩余10gA,则所得溶液中溶质和溶剂的质量比为 20g:100g=1:5;
(2)t2℃时,将26gA物质、29gB物质同时放入100g水中,降温至t1℃A的溶解度是20g,小于26g,析出晶体,B的溶解度是30g,溶液为不饱和溶液,不能析出晶体;
(3)A物质的溶解度受温度影响较大,B的溶解度受温度影响不大,所以A中含有少量B,应用降温结晶法提纯大量A物质;
故答案为:(1)1:5;(2)A;(3)降温结晶(或冷却热饱和溶液).
点评 明确溶解度概念、物质的溶解度受温度影响情况,才能分析提纯物质的方法,难度不大,掌握相关知识即可顺利解答.

练习册系列答案
相关题目
14.二百多年前,哪位法国科学家利用天平进行定量实验,研究了空气的成分( )
| A. |  居里夫人 | B. |  侯德榜 | C. |  诺贝尔 | D. |  拉瓦锡 |
16.下列物质中,属于纯净物的是( )
| A. | 高锰酸钾 | B. | 自来水 | C. | 空气 | D. | 石油 |


 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答: 实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了进行气体制取和性质的探究实验,请回答有关问题:
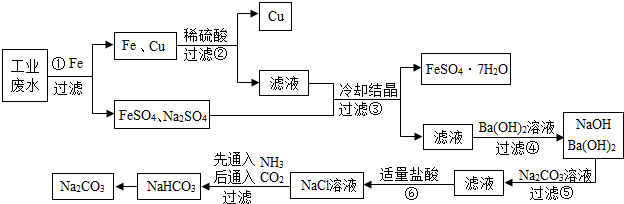
实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了进行气体制取和性质的探究实验,请回答有关问题: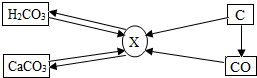 碳和碳的部分化合物间的转化关系如图所示:
碳和碳的部分化合物间的转化关系如图所示: