题目内容
14.通电前水的质量是500克,通电后水的质量变为492.8克,则此过程中生成氢气和氧气的质量分别是多少?分析 根据水减少的质量即为电解的水的质量,结合方程式计算生成氢气和氧气的质量.
解答 解:发生反应的水的质量为500g-492.8g=7.2g
设生成氧气的质量为x,生成的氢气的质量为y,
2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,
36 4 32
7.2g y x
$\frac{36}{7.2g}=\frac{4}{y}=\frac{32}{x}$
解得:x=0.8g,y=6.4g
答:生成氢气0.8g;生成氧气6.4g.
点评 本题主要考查学生化学方程式进行计算和溶液计算的能力,计算时要注意规范性和准确性.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
5.学习、利用化学,可以有效防止安全事故发生.下列有关安全方面的叙述不正确的是( )
| A. | 发现家用天然气泄漏时,绝不能点火或开灯,必须截断气源,打开门窗 | |
| B. | 冬天燃煤取暖一定要打开部分门窗,而燃烧天然气、液化气取暖则不必开门窗 | |
| C. | 久闭的地下室、干涸的深井、深的山洞等地,CO2浓度很高,不能轻易进入 | |
| D. | 煤粉、面粉等固体粉尘与空气充分混合也可能爆炸,故此等场地必须严禁烟火 |
2.图1所示的实验操作中错误的是( )
| A. | 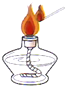 点燃酒精灯 | B. | 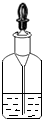 滴管用后直接插回原瓶 | ||
| C. | 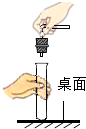 塞橡皮塞 | D. | 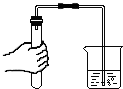 检查气密性 |
9.下列各组分类中,不正确的是( )
| A. | 冰、海波、氯化钠--------常见晶体 | |
| B. | 钢尺、玻璃、石墨--------常见导体 | |
| C. | 蛋白质、维生素、水-----常见营养素 | |
| D. | 溶液、空气、海水----------常见混合物 |
19.半导体工业中.有一句行话:“从沙滩到用户”,即由SiO2制取Si.制取过程中不涉及的化学反应是 ( )
| A. | 2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ | B. | SiO2+2NaOH=Na2SiO3+H2O | ||
| C. | Si+2Cl2$\frac{\underline{\;△\;}}{\;}$SiCl4 | D. | SiCl+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl |
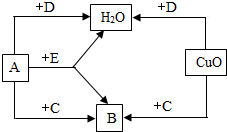 A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,它们之间的转化关系如图所示.
A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,它们之间的转化关系如图所示.
 测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.
测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.