题目内容
19.小明为了探究煅烧了一段时间的石灰石中各成分的质量(其中杂质高温不分解、不溶于水也不与酸反应),进行了如图所示的实验: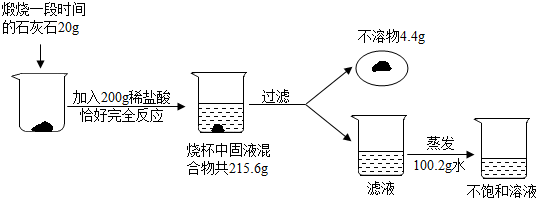
请回答下列问题:
(1)写出有气体生成的化学反应方程式CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)生成气体的质量是4.4g;
(3)写出求解所探究的固体中碳酸钙质量(X)的比例式$\frac{100}{x}$=$\frac{44}{4.4g}$;
(4)该煅烧后的石灰石中各成分的质量最简比是25:14:11;
(5)最终所得的不饱和溶液中,溶质的质量分数为20%;
(6)用上述40t“煅烧一段时间的石灰石”继续充分煅烧,可以得到含杂质的生石灰的质量是31.2t.
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据质量守恒定律计算生成二氧化碳的质量;
(3)根据化学方程式和生成二氧化碳的质量计算参加反应的碳酸钙的质量;
(4)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳进行分析;
(5)根据化学方程式计算反应后溶液中的溶质质量和溶液质量,然后计算溶质的质量分数;
(6)根据石灰石中碳酸钙的含量计算生成氧化钙的质量,然后计算含杂质的生石灰的质量.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑
;
(2)生成二氧化碳的质量为:20g+200g-215.6g=4.4g;
(3)设固体中碳酸钙质量为x,生成氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$=$\frac{111}{y}$
x=10g
y=11.1g
(4)碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56 44
所以煅烧后的石灰石中各成分的质量最简比是100:56:44=25:14:11;
(5)所以混合物氧化钙的质量为:20g-10g-4.4g=5.6g
设氧化钙生成氯化钙的质量为z
CaO+2HCl═CaCl2+H2O
56 111
5.6g z
$\frac{56}{5.6g}$=$\frac{111}{z}$
z=11.1g
所以最终所得的不饱和溶液中,溶质的质量分数为:$\frac{11.1g+11.1g}{215.6g-4.4g-100.2g}$×100%=20%;
(6)40t石灰石中含有碳酸钙质量为:40t×$\frac{10g}{20g}$×100%=20t
设生成二氧化碳的质量为m
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56 44
20t m
$\frac{100}{20t}$=$\frac{44}{m}$
m=8.8t
所以可以得到含杂质的生石灰的质量是40t-8.8t=31.2t.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)4.4g;
(3)$\frac{100}{x}$=$\frac{44}{4.4g}$;
(4)25:14:11;
(5)20%;
(6)31.2t.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案| A. | 小孩了缺乏微量元素钙容易患佝偻病 | |
| B. | 霉变花生含黄曲霉毒素对人体有毒,必须煮熟后才可食用 | |
| C. | 碳纤维、青铜、汽车轮胎都属于复合材料 | |
| D. | 可以用燃烧法区别棉质衣物和真丝织品 |
| A. | 硫在氧气中燃烧发出淡蓝色火焰 | |
| B. | 硫酸铜溶液滴入氢氧化钠溶液中,产生蓝色沉淀 | |
| C. | 将生锈的铁钉放入稀盐酸中,铁锈逐渐消失,溶液颜色变为浅绿色 | |
| D. | 高温条件下木炭还原氧化铜,黑色固体逐渐变成光亮的铜 |
| A. | 铁 | B. | 锌 | C. | 硒 | D. | 碘 |
| A. | 佝偻病 | B. | 贫血症 | C. | 侏儒症 | D. | 甲状腺肿大 |