题目内容
6.请结合如图1所示实验装置,回答有关问题.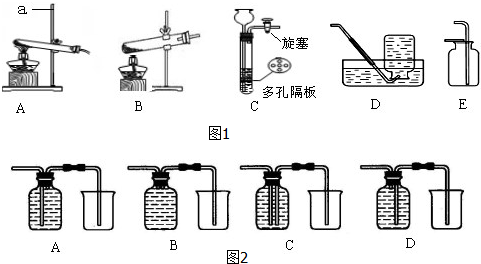
(1)写出装置图1中标号仪器a的名称铁架台.
(2)实验室用氯酸钾和二氧化锰制取较为纯净的氧气,可采用的装置组合为AD,发生反应的化学方程式是2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.
(3)实验室用C装置可以制取氢气,若要使反应停止可采取的操作是关闭导管处的活塞;实验室用过氧化氢溶液和二氧化锰制氧气时用C装置不能(填“能”或“不能”)控制反应的发生和停止.
(4)草酸晶体(H2C2O4•2H2O)加热至101.5℃熔化,150℃左右分解产生H2O、CO和CO2,发生反应的化学方程式为:H2C2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+3H2O,若用加热草酸晶体的方法制取一氧化碳气体,可以选择的气体发生装置是B,为了除去二氧化碳并收集一氧化碳气体,如图2所示装置中最佳的是C(填序号),洗气瓶中装的试剂是氢氧化钠(填化学式)的浓溶液.
(5)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液24mL,水25mL,主要步骤有:计算、混匀、装瓶并贴上标签.
分析 (1)熟记仪器的名称;
(2)根据实验室用氯酸钾制取的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气;
(3)根据装置的特点和药品的状态来分析;
(4)根据加热草酸晶体的方法制取一氧化碳气体的反应物是固体,反应条件是加热,加热固体的正确操作,氢氧化钠会与二氧化碳反应,一氧化碳难溶于水进行分析;
(5)根据溶液配制的知识进行分析,在加水稀释时溶液中溶质的质量不变进行分析.
解答 解:(1)装置图1中标号仪器a的名称是铁架台;故填:铁架台;
(2)实验室用氯酸钾制取的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,排水法收集的氧气较纯净,所以可采用的装置组合为AD,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,故填:AD;2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
(3)用C装置可以制取氢气,若要使反应停止可采取的操作是关闭导管处的活塞;由于隔板上有孔,便于液体的进入,因此固体应该是块状的,而二氧化锰是粉末状的,所以用过氧化氢溶液和二氧化锰制氧气时不能用该装置来控制反应的开始与停止;故填:关闭导管处的活塞;不能;
(4)加热草酸晶体的方法制取一氧化碳气体的反应物是固体,反应条件是加热,所以可以选择的气体发生装置是B,选择该发生装置的原因是:①反应条件需要加热②草酸晶体在101.5℃会熔化因此试管口朝上,氢氧化钠会与二氧化碳反应,一氧化碳难溶于水,所以为了除去二氧化碳并收集一氧化碳气体,下列装置中最佳的是,在洗气瓶中装的试剂是氢氧化钠.故填:B,C,氢氧化钠;
(5)用已配好的质量分数为6%的氯化钠溶液,配制50g质量分数为3%的氯化钠溶液,则需要6%的氯化钠溶液的质量为:$\frac{50g×3%}{6%}$=25g,则需要水的质量为50g-25g=25g,
需要6%的氯化钠溶液的体积为25g÷1.04g/cm3=24mL,需要水的体积为:25g÷1g/cm3=25mL;故填:24,25.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案| A. | H+、Cl-、OH- | B. | Ba2+、NO3-、SO42- | C. | K+、OH-、Na+ | D. | Cu2+、Cl、Na+ |
| A. |  陶瓷花盆 | B. |  真丝围巾 | C. |  大理石地砖 | D. |  塑料保鲜盒 |
①Ni+2HCl═NiCl2+H2↑
②NiO+2HCl═NiCl2+H2O
③NiO2+4HCl═NiCl2+Cl2↑+2H2O
对上述反应的分析判断错误的是( )
| A. | 镍能与氯化铜溶液发生置换反应 | B. | Ni 的金属活动性比 Ag 强 | ||
| C. | Ni 在①的反应中化合价发生了变化 | D. | 反应②和③都是复分解反应 |

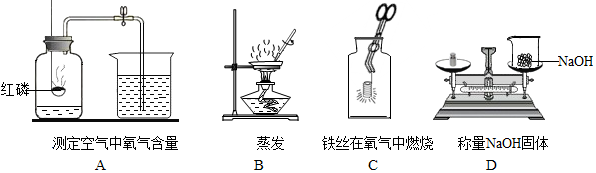
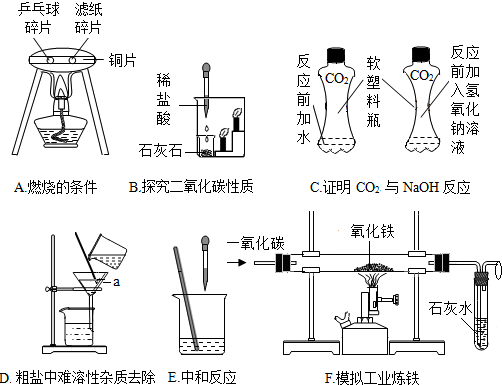
 水是生命之源,也是人类最宝贵的资源.试用你学过的化学知识,回答下列问题:
水是生命之源,也是人类最宝贵的资源.试用你学过的化学知识,回答下列问题: