题目内容
(2011?泉州)为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

请回答:
(1)操作①中被磁铁吸引的金属A是
(2)操作a的名称是
(3)写出步骤②所涉及的化学反应方程式:
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂
a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液.

请回答:
(1)操作①中被磁铁吸引的金属A是
Fe
Fe
;金属B是Cu
Cu
.(2)操作a的名称是
过滤
过滤
;在此过程中需要使用玻璃棒,其作用是引流
引流
.(3)写出步骤②所涉及的化学反应方程式:
Mg+H2SO4=MgSO4+H2↑
Mg+H2SO4=MgSO4+H2↑
,该反应发生的基本类型是:置换反应
置换反应
.(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂
a
a
(填标号).a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液.
分析:根据镁铁铜的性质及与盐反应的规律解答.铁能被磁铁吸引.镁与酸反应,铜与酸不反应.镁能与硫酸铜反应.
解答:解:镁铁铜三种金属中能被磁铁吸引的是铁,故A为铁,镁和铜中加入硫酸,镁与硫酸反应生成氢气和硫酸镁,而铜与稀硫酸不反应过滤即可得到金属B为铜,硫酸镁溶液蒸发水分得到硫酸镁固体.步骤②中除了加入硫酸溶液外,还可选用的试剂是加入硫酸铜,镁与硫酸铜反应生成硫酸镁.
故答案为:
(1)Fe,Cu;
(2)过滤,引流;
(3)Mg+H2SO4=MgSO4+H2↑,置换反应;
(4)a.
故答案为:
(1)Fe,Cu;
(2)过滤,引流;
(3)Mg+H2SO4=MgSO4+H2↑,置换反应;
(4)a.
点评:明确金属的物理性质及化学性质是解答本题关健.熟记金属活动性顺序表,氢前金属与酸反应,活动性强的金属能置换活动性弱的金属.

练习册系列答案
相关题目
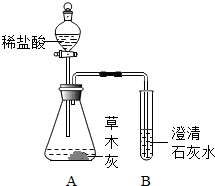 (2011?泉州)小云同学在整理厨房时不小心将一瓶醋打翻,醋洒在火炉旁的一堆草木灰上,发现有大量的气泡生成.激发了兴趣,于是他决定与学习小组的同学,对草木灰的成分进行探究.
(2011?泉州)小云同学在整理厨房时不小心将一瓶醋打翻,醋洒在火炉旁的一堆草木灰上,发现有大量的气泡生成.激发了兴趣,于是他决定与学习小组的同学,对草木灰的成分进行探究. (2011?泉州)如图是元素周期表中的一部分,下列有关说法中正确的是( )
(2011?泉州)如图是元素周期表中的一部分,下列有关说法中正确的是( ) (2011?泉州)如图为一个化学反应的微观示意图,其中“
(2011?泉州)如图为一个化学反应的微观示意图,其中“ ”表示H原子,“
”表示H原子,“ ”表示Br原子,下列有关说法中正确的是( )
”表示Br原子,下列有关说法中正确的是( )