题目内容
17. 在一烧杯中盛有12.2gCaCO3和CaCl2的粉末状混合物,向其中加入188.8g水,使混合物中的可溶物完全溶解,然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图X所示;请根据题意回答下列问题:
在一烧杯中盛有12.2gCaCO3和CaCl2的粉末状混合物,向其中加入188.8g水,使混合物中的可溶物完全溶解,然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图X所示;请根据题意回答下列问题:(1)在滴入稀盐酸的过程中,观察到的明显实验现象是:①固体溶解②产生气泡.
(2)当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)CaCl2.
(3)当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液的质量.(计算结果精确至0.1g)
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的信息和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)在滴入稀盐酸的过程中,碳酸钙和稀盐酸不断反应,观察到固体溶解,产生气泡.
故填:固体溶解;产生气泡.
(2)当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是原混合物中的氯化钙和反应生成的氯化钙.
故填:CaCl2.
(3)设生成二氧化碳质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
146g×10% x
$\frac{73}{146g×10%}$=$\frac{44}{x}$,
x=8.8g,
此时烧杯中所得不饱和溶液的质量为:12.2g+188.8g+146g-8.8g=338.2g,
答:此时烧杯中所得不饱和溶液的质量为338.2g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.初中化学学习了很多化学反应,下列有关叙述中,不正确的是( )
| A. | 中和反应生成盐和水,但生成盐和水的反应不一定是中和反应 | |
| B. | 置换反应前后一定会有元素化合价的改变 | |
| C. | 两种化合物生成另外两种新化合物的反应一定是复分解反应 | |
| D. | 化合反应的生成物一定不是单质 |
5.双氧水的主要成分是过氧化氢(化学式为H2O2),医疗上常使用2.5-3.5%的过氧化氢的水溶液来处理伤口创面或清洗化脓性疮口,下面对过氧化氢的说法合理的是( )
| A. | 过氧化氢是由氢气和氧气组成的化合物 | |
| B. | 过氧化氢中氧元素的化合价是-1价 | |
| C. | 过氧化氢由两个氢原子和两个氧原子组成 | |
| D. | 过氧化氢分子中氢、氧元素的个数比为1:1 |
12.某实验室的废液中,可能含有CuCl2、NaCl、Na2SO4、Na2CO3、Ba(NO3)2中的一种或多种,某同学取该废液观察为无色溶液,向其中滴加BaCl2溶液产生白色沉淀,继续滴加稀硝酸无明现象,根据以上实验现象分析,下列推断正确的是( )
| A. | 一定存在Na2SO4 | B. | 可能存在Na2CO3 | C. | 一定存在CuCl2 | D. | 一定不存在NaCl |
7. 某件衣服标签的部分内容如图,以下说法错误的是( )
某件衣服标签的部分内容如图,以下说法错误的是( )
 某件衣服标签的部分内容如图,以下说法错误的是( )
某件衣服标签的部分内容如图,以下说法错误的是( )| A. | 羊毛是天然纤维 | |
| B. | 涤纶是合成纤维 | |
| C. | 可用灼烧的方法来区分羊毛和涤纶 | |
| D. | 合成纤维的吸水性和透气性要比天然纤维好 |
 和
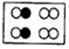
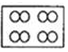
和 分别表示不同元素的原子,其中表示单质的是( )
分别表示不同元素的原子,其中表示单质的是( )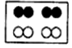

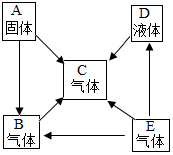 已知A、B、C、D、E是初中化学中五种常见的纯净物,五种物质中 A、E为单质其余都为化合物,由于条件不同A和E反应可生成B也可生成C.五种物质在一定条件下的转化关系如右下图所示(“-”表示相连物质间能反应,“→”表示物质间可转化,部分反应物和生成物没有列出).试推断并回答相关问题:
已知A、B、C、D、E是初中化学中五种常见的纯净物,五种物质中 A、E为单质其余都为化合物,由于条件不同A和E反应可生成B也可生成C.五种物质在一定条件下的转化关系如右下图所示(“-”表示相连物质间能反应,“→”表示物质间可转化,部分反应物和生成物没有列出).试推断并回答相关问题: