题目内容
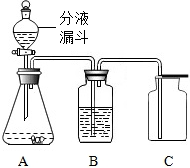 过氧化氢(H2O2)溶液在MnO2作催化剂的条件下,能迅速分解生成O2和H2O.分液漏斗可以通过调节控制液体的滴加速度.现欲制取干燥而纯净的氧气,可以采用如图所示装置:
过氧化氢(H2O2)溶液在MnO2作催化剂的条件下,能迅速分解生成O2和H2O.分液漏斗可以通过调节控制液体的滴加速度.现欲制取干燥而纯净的氧气,可以采用如图所示装置:回答下列问题:
(1)分液漏斗中盛放的物质是
(2)装置B中的药品是
(3)A中发生反应的化学方程式是
(4)用该实验代替加热KMnO4制取O2,优点是(填序号)
①生成物只有氧气 ②不需加热 ③生成的氧气多
(5)若改变装置A中的药品,此套装置还可以用来制取
考点:氧气的制取装置,氧气的收集方法,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从过氧化氢溶液是液体去分析;
(2)从题目要求制取干燥而纯净的氧气,故B装置中应为干燥剂(除去水分)去分析;
(3)从用过氧化氢和二氧化锰混合制取氧气时,生成氧气的同时还有水生成,由于是一种物质生成两种或两种以上的物质,所以属于分解反应去分析;
(4)①从用过氧化氢和二氧化锰混合制取氧气,生成物中除了氧气还有水分去分析;
②从用过氧化氢和二氧化锰混合制取氧气,不需加热,可以节约能源去分析;
③由于没有说明过氧化氢溶液和高锰酸钾的质量去分析;
(5)从A装置是固体和液体反应且不需加热制取气体去分析.
(2)从题目要求制取干燥而纯净的氧气,故B装置中应为干燥剂(除去水分)去分析;
(3)从用过氧化氢和二氧化锰混合制取氧气时,生成氧气的同时还有水生成,由于是一种物质生成两种或两种以上的物质,所以属于分解反应去分析;
(4)①从用过氧化氢和二氧化锰混合制取氧气,生成物中除了氧气还有水分去分析;
②从用过氧化氢和二氧化锰混合制取氧气,不需加热,可以节约能源去分析;
③由于没有说明过氧化氢溶液和高锰酸钾的质量去分析;
(5)从A装置是固体和液体反应且不需加热制取气体去分析.
解答:解:(1)由于过氧化氢溶液是液体,所以分液漏斗中的药品应为过氧化氢溶液;故答案为:过氧化氢溶液;
(2)由于题目要求制取干燥而纯净的氧气,故B装置中应为干燥剂(除去水分),常用的液体干燥剂是浓硫酸;故答案为:浓硫酸;
(3)用过氧化氢和二氧化锰混合制取氧气时,生成氧气的同时还有水生成,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰的作用是起了催化剂的作用也就是催化作用.所以二氧化锰就应该作为反应条件写在等号的上方,故化学方程式为:2H2O2
2H2O+O2↑,由于是一种物质生成两种或两种以上的物质,所以属于分解反应;故答案为:2H2O2
2H2O+O2↑ 分解反应;
(4)①用过氧化氢和二氧化锰混合制取氧气,生成物中除了氧气还有水分;故错误;
②用过氧化氢和二氧化锰混合制取氧气,不需加热,可以节约能源,故是优点;故正确;
③由于没有说明过氧化氢溶液和高锰酸钾的质量,所以无法比较二者生成的氧气多少;故错误;
故答案为:②;
(5)由于A装置是固体和液体反应且不需加热制取气体;若改变装置A中的药品,换成石灰石和稀盐酸就可以用来用来制取二氧化碳气体;故答案为:二氧化碳.
(2)由于题目要求制取干燥而纯净的氧气,故B装置中应为干燥剂(除去水分),常用的液体干燥剂是浓硫酸;故答案为:浓硫酸;
(3)用过氧化氢和二氧化锰混合制取氧气时,生成氧气的同时还有水生成,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰的作用是起了催化剂的作用也就是催化作用.所以二氧化锰就应该作为反应条件写在等号的上方,故化学方程式为:2H2O2
| ||
| ||
(4)①用过氧化氢和二氧化锰混合制取氧气,生成物中除了氧气还有水分;故错误;
②用过氧化氢和二氧化锰混合制取氧气,不需加热,可以节约能源,故是优点;故正确;
③由于没有说明过氧化氢溶液和高锰酸钾的质量,所以无法比较二者生成的氧气多少;故错误;
故答案为:②;
(5)由于A装置是固体和液体反应且不需加热制取气体;若改变装置A中的药品,换成石灰石和稀盐酸就可以用来用来制取二氧化碳气体;故答案为:二氧化碳.
点评:实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;考查了实验室制取氧气的反应原理,及注意事项,是考试的重点也是中考的重点.

练习册系列答案
相关题目
生活中常见的下列现象,都属于化学变化的是( )
| A、汽油挥发 酒精燃烧 |
| B、铜铁生锈 食物腐烂 |
| C、水分蒸发 滴水成冰 |
| D、铁铸成锅 蜡烛燃烧 |
下列安全常识中.不正确的是( )
| A、家中煤气泄露--向室内洒水 |
| B、在加油站附近-一禁止吸烟 |
| C、煤矿中瓦斯气体泄露--严禁开关电器 |
| D、逃离火灾现场--用湿毛巾捂住口鼻 |

 某环保小组监测到一工厂向河中排放的酸性废液中含有CuCl2.为了测定废液中CuCl2的质量分数.该小组取了100g废液,逐滴滴入NaOH溶液至过量.测得生成Cu(OH)2沉淀与所加NaOH溶液的质量关系如图.
某环保小组监测到一工厂向河中排放的酸性废液中含有CuCl2.为了测定废液中CuCl2的质量分数.该小组取了100g废液,逐滴滴入NaOH溶液至过量.测得生成Cu(OH)2沉淀与所加NaOH溶液的质量关系如图.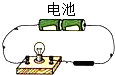 如图实验说明石墨具有
如图实验说明石墨具有