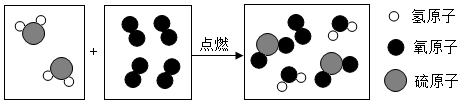
题目内容
4.某金属冶炼厂在生产过程中产生了一定量的含铜废料.化学兴趣小组利用稀硫酸和铁粉分离回收铜,并获得硫酸亚铁晶体.其设计方案如图所示: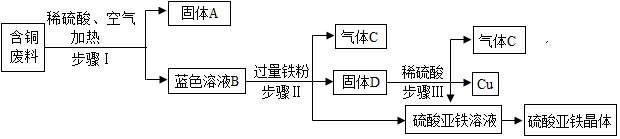
则下列说法正确的是( )
| A. | 蓝色溶液B中的溶质是硫酸铜 | |
| B. | 步骤II是的主要操作是过滤 | |
| C. | 固体D属于纯净物 | |
| D. | 最终获得纯铜的质量比废料中铜的质量大 |
分析 铜和稀硫酸在氧气的作用下加热生成硫酸铜和水,硫酸铜能和铁反应生成硫酸亚铁和铜,稀硫酸能和铁反应生成硫酸亚铁和氢气.
解答 解:A、加入过量铁粉时产生气泡,说明步骤Ⅰ中稀硫酸过量,因此蓝色溶液B中的溶质是硫酸铜和硫酸,该选项说法不正确;
B、步骤II是的主要操作是过滤,通过过滤把液体和固体分离,该选项说法正确;
C、固体D中含有铜和铁,属于混合物,该选项说法不正确;
D、最终获得纯铜的质量和废料中铜的质量相等,如果过程中铜元素有流失时,最终获得纯铜的质量比废料中铜的质量小,该选项说法不正确.
故选:B.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.分类是学习化学的方法之一,下列各组物质是按单质,氧化物,混合物进行分类的是( )
| A. | 液氧 熟石灰 空气 | |
| B. | 活性炭 酒精 碘盐 | |
| C. | 生铁 干冰 矿泉水 | |
| D. | 金刚石 冰 高锰酸钾制氧气的剩余固体 |
12.为测定某BaCl2溶液的溶质质量分数,进行如下实验:取208g该溶液与烧杯中,加入2g稀硝酸溶液酸化,无任何现象.然后将60g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽略不计).数据如表:
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为46.6g.
(2)该BaCl2溶液总溶质的质量分数为多少?
| 第1次 | 第2次 | 第3次 | |
| 加入硫酸溶液的质量/g | 20 | 20 | 20 |
| 过滤后溶液的质量/g | 210 | 210 | 223.4 |
(1)该实验过程中产生沉淀的总质量为46.6g.
(2)该BaCl2溶液总溶质的质量分数为多少?
9.下列描述完全正确的是( )
| A. | 可用水鉴别石灰石与食盐 | |
| B. | 人体缺乏维生素C会引起夜盲症 | |
| C. | 在化学反应中只有燃烧才能放出热量 | |
| D. | 合金属于合成材料 |
16.下列物质中属于纯净物的是( )
| A. | 加碘食盐 | B. | 烧碱 | C. | 矿泉水 | D. | 浓硫酸 |
13.下列有关水的净化和处理,说法正确的是( )
| A. | 生活污水应集中处理,达标后再排放 | |
| B. | 过滤能除去水中所有的杂质 | |
| C. | 硬水经活性炭吸附后变成软水 | |
| D. | 电解水生成氢气和氧气的质量比约为2:1 |
14.下列相关实验方法能达到目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别稀硫酸和硫酸钠溶液 | 滴加酚酞 |
| B | 鉴别氢气和甲烷 | 点燃,火焰上罩一个冷而干燥的烧杯 |
| C | 除去KCl固体中的MnO2 | 溶解、过滤和蒸发 |
| D | 除去NaCl溶液中少量的Na2CO3 | 加入足量的石灰水,过滤 |
| A. | A | B. | B | C. | C | D. | D |
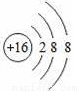 表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+;⑦最简单的有机化合物:C2H5OH。其中,正确的是( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+;⑦最简单的有机化合物:C2H5OH。其中,正确的是( )