题目内容
17.下列实验现象的描述不正确的是( )| A. | 硫在空气中燃烧,发出淡蓝色火焰 | |
| B. | 木炭在氧气中燃烧,发出白光 | |
| C. | 对着干燥玻璃片呼气,玻璃片上有水雾产生 | |
| D. | 石蜡在空气中燃烧时,生成水和二氧化碳 |
分析 A、根据硫在空气 中燃烧的现象进行分析判断.
B、根据木炭在氧气中燃烧的现象进行分析判断.
C、根据呼出气体中含有较多的水蒸气进行分析判断.
D、根据石蜡在空气中燃烧的现象进行分析判断.
解答 解:A、硫在空气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体,说法正确;
B、木炭在氧气中燃烧 发出白光,生成无色气体,说法正确;
C、呼出气体中含有较多的水蒸气,所以对着干燥玻璃片呼气,玻璃片上有水雾产生,说法正确;
D、石蜡在空气中燃烧生成水和二氧化碳是实验结论,不是实验现象,故错误;
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象、呼出气体的成分即可正确解答;在描述物质燃烧的现象时,需要注意实验结论和实验现象的区别.

练习册系列答案
相关题目
8.如表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
(1)在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.改变温度使KNO3析出,NaCl不析出,则温度T(℃)的范围是20℃~70℃(硝酸钾和氯化钠溶解度互不影响),当改变温度的过程中NaCl在溶液中恰好饱和时,溶液中KNO3和溶剂的质量比为8:25.
(2)向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.

①~⑤中溶液为饱和状态的是②⑤(填序号①-⑤,①-⑤中A溶液中溶质质量分数相等的是④⑤(填序号①-⑤).
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.

| 资料:A的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
9.小红发现自己家的铁锅在与水面接触的部位最易生锈;小兰发现自己的铜制眼镜框表面出现了绿色的铜锈;
小花发现吃剩苹果的果肉上会产生一层暗褐色物质,好象生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:(1)回忆已有知识:铁生锈的条件是与水和氧气接触.
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成暗褐色的物质.
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下,装置Ⅱ中氢氧化钠溶液和碱石灰的作用是吸收二氧化碳;写出装置Ⅱ氢氧化钠溶液中发生反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(4)由实验可知:铜生锈是铜与水、氧气、二氧化碳等物质共同作用的结果.
【得出结论】(5)经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气有关.
小花发现吃剩苹果的果肉上会产生一层暗褐色物质,好象生了“锈”一般.
【提出问题】:这三种物质“生锈”的原因是什么?
【收集证据】:(1)回忆已有知识:铁生锈的条件是与水和氧气接触.
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成暗褐色的物质.
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下,装置Ⅱ中氢氧化钠溶液和碱石灰的作用是吸收二氧化碳;写出装置Ⅱ氢氧化钠溶液中发生反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
| 实验 装置 | 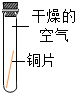 | 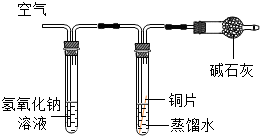 | 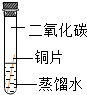 | 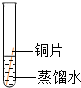 |
| 实验 现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面 附近锈蚀最严重 |
【得出结论】(5)经过交流讨论,三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与氧气有关.