题目内容
9.下列图形能正确反映实验事实的是( )| A. | 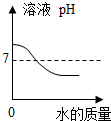 氢氧化钠溶液中加水 | |
| B. | 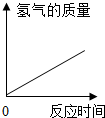 稀硫酸中加入铁粉 | |
| C. |  充分加热氯酸钾和二氧化锰的混合物 | |
| D. | 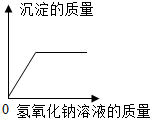 硫酸铜和硫酸混合液滴入氢氧化钠溶液 |
分析 A、氢氧化钠溶液显碱性,加水稀释溶液的碱性减弱,溶液的pH减小,据此进行分析判断.
B、根据铁能与稀硫酸反应生成硫酸亚铁和氢气,进行分析判断.
C、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,据此进行分析判断.
D、向硫酸铜和硫酸混合液中加入氢氧化钠溶液时,先与硫酸反应,开始时不会生成沉淀,硫酸消耗完后再与硫酸铜应会生成氢氧化铜沉淀.
解答 解:A、氢氧化钠溶液显碱性,加水稀释溶液的碱性减弱,溶液的pH减小,但加再多的水溶液也呈碱性,溶液的pH也会大于7,故图象与实验操作过程不对应.
B、铁能与稀硫酸反应生成硫酸亚铁和氢气,完全反应后质量不变,生成气体的量先是零,再不断上升,最后形成一条水平直线,故图象与实验操作过程不对应.
C、氯酸钾中钾元素的质量分数不为0;氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应后氧气的逸出,剩余固体的质量减少,反应前后钾元素的质量不变,则混合物中钾元素的质量分数增大,完全反应后不变,最后形成一条水平直线,故图象与实验操作过程对应.
D、向硫酸铜和硫酸混合液中加入氢氧化钠溶液时,先与硫酸反应,开始时不会生成沉淀,硫酸消耗完后再与硫酸铜应会生成氢氧化铜沉淀,故沉淀的量先是零,再不断上升,最后形成一条水平直线;故图象与实验操作过程不对应.
故选:C.
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
19.用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15.0克干燥样品进行实验:
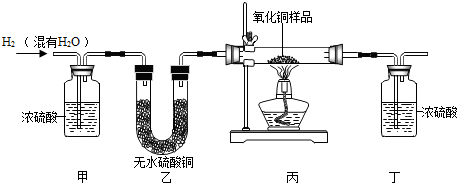
(1)写出氢气还原氧化铜的化学方程式H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
(2)在实验中,乙装置的作用是检验甲装置是否除尽氢气中水蒸气.
(3)准确称取完全反应前后装置丙和丁的质量如表:
某学生甲根据装置丙的质量变化进行计算,得到氧化铜样品的纯度为76.7%,某学生乙根据丁的质量变化同样可以计算,得到氧化铜样品的纯度比甲的结果大于
(填“大”、“小”或“相等”).
(3)比较两种计算结果,有的同学认为学生甲结果较合理准确;有的同学认为学生乙结果较合理准确.经讨论分析,最后达成共识:学生乙结果存在不合理之处,原因是装置丁可吸收空气中的水蒸气,造成结果偏高.学生甲结果只有达到下列条件才足够准确:装置乙现象是固体保持白色、装置丙现象是由黑色完全变红色,出现这些现象后移去酒精灯,要继续通往氢气,直到丙中试管冷却.

(1)写出氢气还原氧化铜的化学方程式H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
(2)在实验中,乙装置的作用是检验甲装置是否除尽氢气中水蒸气.
(3)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
(填“大”、“小”或“相等”).
(3)比较两种计算结果,有的同学认为学生甲结果较合理准确;有的同学认为学生乙结果较合理准确.经讨论分析,最后达成共识:学生乙结果存在不合理之处,原因是装置丁可吸收空气中的水蒸气,造成结果偏高.学生甲结果只有达到下列条件才足够准确:装置乙现象是固体保持白色、装置丙现象是由黑色完全变红色,出现这些现象后移去酒精灯,要继续通往氢气,直到丙中试管冷却.
4.有关实验现象的描述错误的是( )
| A. | 硫在空气中燃烧发出淡蓝色火焰 | |
| B. | 镁在空气中燃烧:发出耀眼白光,放出热量,产生大量的白雾 | |
| C. | 把盛有浓盐酸的试剂瓶的盖子打开后,瓶口上方会出现白雾 | |
| D. | 向硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀 |
18.属于钾肥的是( )
| A. | NH3•H2O | B. | KCl | C. | NH4Cl | D. | Ca3(PO4)2 |
19.下列说法正确的是( )
| A. | 空气的成分按体积计算氮气最多 | |
| B. | 催化剂只能加快化学反应速率 | |
| C. | 植物叶片发黄应施加磷肥 | |
| D. | 碳酸氢钠俗称苏打,是发酵粉成分之一 |